缺血性卒中:预后与结局评价|临床实践
时间:2023-04-14 11:14:14 热度:37.1℃ 作者:网络
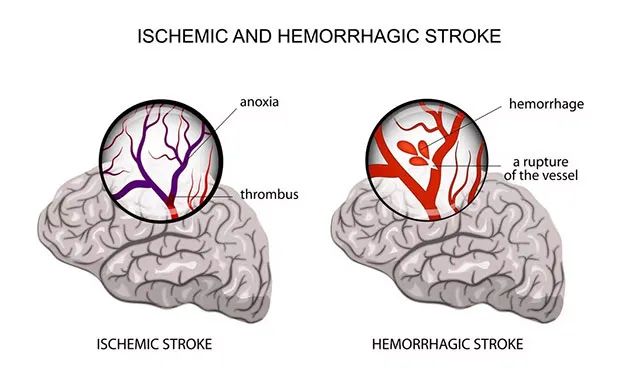
缺血性卒中是多样性疾病,具有高发病率、高致残率、高死亡率、高复发率等特点。美国统计数据显示每40分钟增加1例卒中患者,每年有795000例新发和复发卒中患者。基于多种因素,卒中的治疗效果受到了限制。目前我国脑血管疾病发病率为120/10万~180/10万,由于人口老龄化日益严重,其发病率逐渐升高。随着科学研究的不断深入,发现急性期积极干预可改善病人脑组织结构和功能状态,实现“脑可塑”。
涉及卒中结局的几个因素:
-
急性出血的存在;
-
血栓位置及程度;
-
可逆性缺血组织;
-
低灌注组织的存在,有后续梗死风险;
-
侧支循环的情况;
-
再通时间。
最理想状态就是:小核心、侧支良好、近端血栓。在这里引入3C方法:核心(core)、血栓情况(clot)、侧支循环(collaterals)。
1. 核心
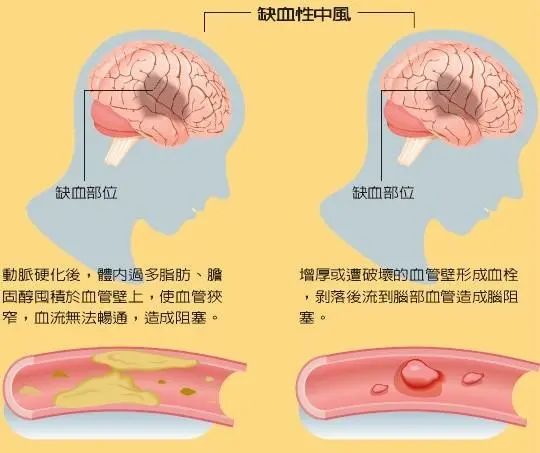
脑梗死核心平均生长速度5.4ml/h,其速度快慢取决于侧支循环程度。最近有研究确定了一个阈值:核心>70ml,即使再通率50%,预后也较差,平均增长为114ml;核心<70ml与良好预后相关,64%患者MRS评分0~2分,梗死体积增长较慢。DEFUSE试验证实磁共振弥散像(DWI)>80ml,再通不良率更高。初始梗死可能预测恶性卒中进展,Thomalla等发现恶性大脑中动脉(MCA)综合征,发病6h内DWI体积>82ml。磁共振(MR)的DWI序列评估核心体积最可靠,但是可能会延误治疗时间。
DWI可用于急性缺血性卒中的早期诊断,特别是最初12h,在评估核心体积(尤其是>82ml的恶性大脑中动脉梗死)的不良预后中高度特异。研究人员把核心分为小(<10ml)、中(10~100ml)、大(>100ml),大核心患者的症状性出血风险增加5~8倍。CT的主要优点是广泛的获取和快速的获取速度。
在超急性期,通常要求进行非增强CT(NECT)扫描以排除或确认出血,它对这种适应证非常敏感。患者一旦病情稳定,就应该进行NECT扫描,与CT动脉成像(CTA)和CT灌注成像(CTP)的多模式来评估血管闭塞部位、梗死核心,以及可挽救的脑组织和侧支循环程度。与MR相比,尽管多了辐射和对比剂的担忧,但能显示与DWI类似的核心组织,且能更好地显示早期缺血性组织(该部分组织仅在早期再通时可逆)。
ASPECT评分可以评估大脑中动脉缺血范围。ASPECT8~10分表示没有或很小的核心;≤4分,核心范围超过大脑中动脉1/3范围或≥80ml。在Canadian Alteplaseforstoke Effective试验中:936例患者ASPECT评分是强预测因子,分数越低,预后越差。ASPECT0~2分与较大梗死体积有关。多元回归分析提示:ASPECT8~10分与MRS0~2相关;≤4分与死亡相关;≤5分与症状性颅内出血相关。
2.血栓部位及侧支循环
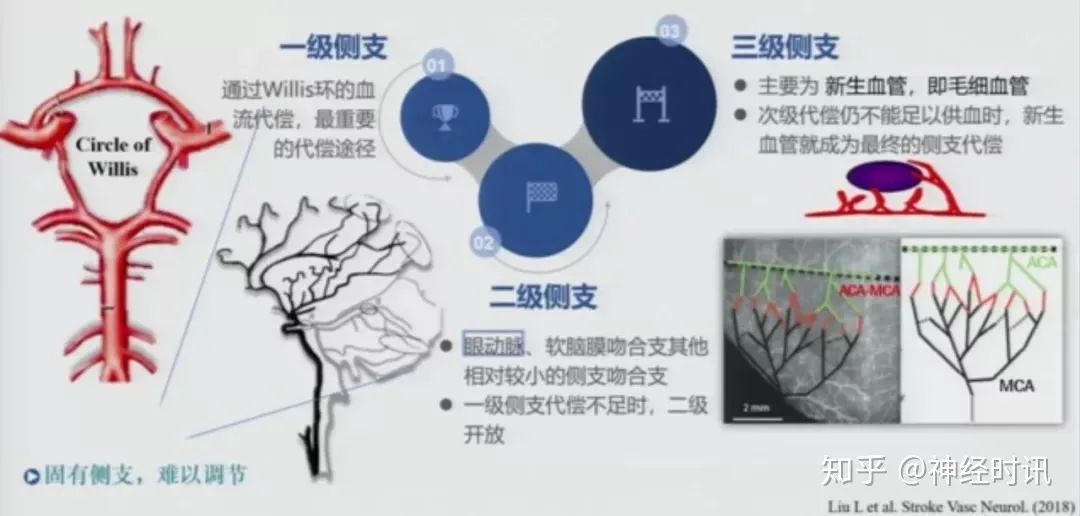
CT血管造影除了可以评估闭塞血管外,还可以看血管钙化和动脉硬化,评估软脑膜侧支代偿。侧支决定了核心增长的速度,影响出血转化可能。研究表明较差的侧支多有较大的DWI病变体积及高NIHSS评分,预后不良。基于CT造影的CBS评分系统适用于前循环,评分越高,预后越好,死亡可能性越小,最终梗死面积小且出血转化率低。同时早期征象如大脑中动脉致密征的存在也可以提示闭塞部位。MCA近端闭塞患者,闭塞血管CT值与对侧动脉CT值比值是血管再通最强预测因子。
Hounsfield unit ratio(rHu)<1.382具有灵敏性及特异性,可用于静脉溶栓后是否再通检测。脑血管造影是评估侧支的“金标准”,建立ISTNASR分级标准,侧支差则出血风险高。其优点在于能评估血管狭窄及解剖,还可以排除是否存在血管炎等其他病变,同时可以结合动脉内溶栓和血管成形术。但急性卒中患者使用较少,主要原因在于CTA、MRA等无创检查也可以评估且存在造影相关的卒中风险。
3. 半暗带
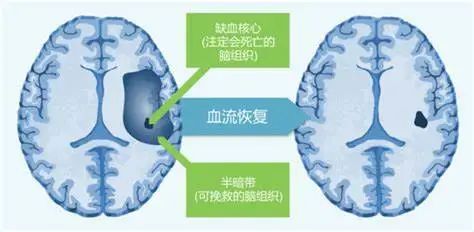
半暗带的临床应用尚存在争议。目前提出的假设是:识别有风险的组织允许治疗窗口>4.5h,区别患者可获益还是对治疗不利。有证据表明,无论是否再通治疗,良好的半暗带多有好的预后。患者通过多种途径适应血管闭塞,无论治疗方案如何都有良好结果,对卒中分层治疗有指导作用。半暗带在MR上以反映通过扩散-灌注不匹配(DPMM)估计的“有风险”组织。理论上认为,在DWI上没有受限制的水运动,但在灌注加权成像(PWI)上确实具有破坏的血液输送组织,表示为血液流动恢复则不会进化为完全脑梗死的可挽救的脑组织。
MRRESCUE和DEFUSE2试验主要针对MR不匹配成像:DEFUSE2试验使用DPMM根据阈值定义“目标数据”,而MRRESCUE试验使用DPMM根据等式识别“半暗带”。DEFUSE结论表明达峰时间(Tmax)与扩散错配,尽管再灌注,大核心或大灌注缺损的不匹配患者具有不利结果。Tmax>8s,体积>100ml是恶性梗死的征象,预后不良。MRRESCUE没有发现DPMM可以识别出对血管内治疗有益的患者。这两项试验导致相反结论的原因:入组偏倚和再通率差异。然而,这些试验能够确定血管内治疗的潜在益处,取决于对危险组织和核心梗死的准确和无偏见的估计。如果定义高估了风险组织并低估了核心梗死,则可以解释MRRESCUE的阴性结果。这提示MR用于检测半暗带实用性有限,提供不了闭塞血管及代偿。
CTA可以显示闭塞血管,通过MTT、CBV、CBF等值的变化评估核心组织、半暗带。依据CTA进行早期核心评估,比MR更加准确。CTA灌注可以作为卒中患者治疗的选择工具,从治疗中获益的各种假设,评估预后。ECASS研究发现血流灌注与预后、出血风险相关:静脉溶栓215例患者,低灌注区域均有改善,其中52例有大低灌注区,出血致命性出血风险增加和预后不良。
4. 时间
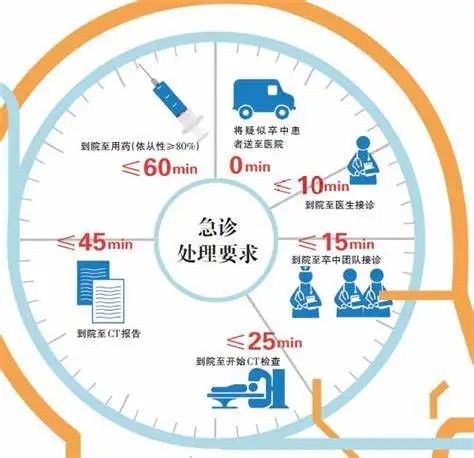
“时间就是大脑”,不必要的成像不能减缓急性脑卒中治疗。严重缺血每分钟平均可损失大约200万个神经元,所以绝对不能延迟“血栓破坏”再灌注治疗,甚至不能耽误几分钟去进行诊断成像,这对于安全有效的治疗分诊并非绝对必要。
有两点值得注意:
(1)基于多种因素,如缺血预处理和侧支血流的质量,神经元在个体患者中死亡的实际速率存在巨大差异。
(2)任何单一成像参数都反映了梗死发展演变中的“时间快照”,不能用于估计缺血持续时间,这是测量特征的参数组合。
具有不同时间进程的缺血组织有可能比任意“时钟时间”更能准确地评定梗死的真实“生理年龄”。此外,在呈现具有未知起效时间(“醒后”卒中)的多数脑卒中患者比率可以受益于更合理的影像学成像,而不是基于时间的治疗选择的特殊类别。
目前正在进行II期临床试验,通过使用液体衰减反转恢复(FLAIR)和弥散加权成像之间的不匹配来确定静脉t-PA对未知起效时间的脑卒中的安全性-扩散加权成像对早期(3h)细胞毒性水肿更敏感,FLAIR对后期(通常为0.6h)血管源性水肿更敏感。用影像学组织时间代替发病时间窗,可开展超时间窗再灌注治疗,使更多患者能接受最合理的治疗方式。
参考文献:
1.吴宇飞.急性缺血性卒中影像学综述[J].现代实用医学,2020,32(06):607-609.
2.王平平,等.神经影像学对缺血性脑血管病复发风险评估的研究进展[J].中西医结合心脑血管病杂志,2020,18(18):3026-3029.


