论文解读|Hu N/ Qin L/Yuan Y教授团队揭示载有BMSC来源凋亡囊泡的纤维支架促进伤口愈合的机制
时间:2025-04-03 12:10:57 热度:37.1℃ 作者:网络
巨噬细胞是介导伤口愈合的关键细胞,伤口微环境会影响巨噬细胞极化为早期的促炎M1表型或后期的促愈合M2表型。巨噬细胞M2表型极化功能障碍、巨噬细胞数量减少以及抗炎和促血管新生能力降低是导致伤口长期不愈合的原因。间充质干细胞(MSCs)通过分泌细胞外囊泡传递内源性调节因子,辅助组织修复和再生。既往研究表明,BMSC来源的凋亡囊泡可诱导巨噬细胞极化为M2表型,减轻炎症反应,并增强成纤维细胞的迁移和增殖能力。
重庆医科大学的Ning Hu/Leilei Qin/Yonghua Yuan教授团队在本刊发表了题为“Fibrous scaffolds loaded with BMSC-derived apoptotic vesicles promote wound healing by inducing macrophage polarization”的研究论文。该研究设计了一种载有BMSC来源凋亡囊泡(ABs)的聚己内酯(PCL)纤维支架,通过体外和体内实验,探究了负载BMSC-AB的静电纺丝PCL纤维支架的伤口愈合效果及巨噬细胞极化潜力。
01 PCL-BMSC-ABs对M0巨噬细胞向M2表型转化的影响
研究团队从小鼠骨髓分离BMSCs,诱导凋亡获取ABs。团队还制备了PCL纤维支架,成功负载ABs。研究团队将RAW264.7巨噬细胞与PCL-BMSC-ABs共孵育,发现ABs显著提高M2标志物(精氨酸酶-1、CD206)表达和VEGF分泌,促进M0巨噬细胞向抗炎M2表型转化。流式细胞术显示,共孵育48小时后,M0巨噬细胞向M2表型转化比例达69.2%(图1)。

图1 PCL-BMSC-ABs引导M0型巨噬细胞体外极化为M2型巨噬细胞(原文中Figure 2)
02 miR-21a-5p在ABs介导的巨噬细胞极化中的作用
通过miRNA测序分析,研究团队发现BMSC-ABs中含有353种已知的miRNAs,其中miR-21a-5p表达量最高。双荧光素酶实验验证了miR-21a-5p与靶基因CCL-1的结合。进一步的实验表明,miR-21a-5p抑制剂能够显著降低M2标志物的表达,而CCL-1受体拮抗剂则部分阻断了ABs的极化作用(图2)。这表明miR-21a-5p通过靶向CCL-1在ABs介导的巨噬细胞极化中发挥关键作用。
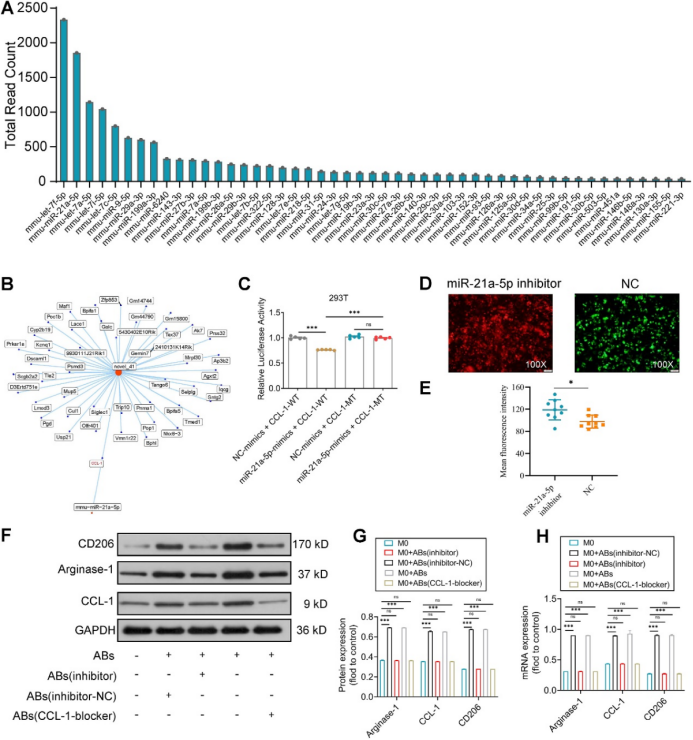
图2 PCL-BMSC-ABs驱动巨噬细胞(Mϕs)向M2型巨噬细胞(M2-Mϕs)分子重编程的miRNA测序分析(原文中Figure 3)
03 PCL-BMSC-ABs对体外炎症和成纤维细胞迁移的促进作用
研究团队通过Bio-Plex蛋白芯片分析了不同处理组巨噬细胞分泌的细胞因子和趋化因子水平,发现PCL-BMSC-ABs处理组的抗炎细胞因子(如IL-4、IL-10、CCL-1和TGF-b)和血管指标(如VEGF和vWF)显著高于其他组。此外,通过Transwell共培养实验发现,PCL-BMSC-ABs处理的巨噬细胞能够显著促进成纤维细胞的迁移能力(图3),表明ABs不仅能够调节巨噬细胞的极化,还能够促进成纤维细胞的迁移,从而加速伤口愈合。

图3 PCL负载的M2细胞的体外抗炎和促成纤维细胞迁移效应(原文中Figure 4)
04 体内实验验证PCL-BMSC-ABs的促愈合效果
在C57BL/6小鼠的皮肤创伤模型中,研究团队发现PCL-BMSC-ABs能够显著促进伤口愈合,减少炎症细胞浸润,并促进胶原纤维形成。免疫组化染色结果显示,PCL-BMSC-ABs处理组中M2标志物(如精氨酸酶)的表达显著增加,而M1标志物(如iNOS)的表达则显著降低。此外,PCL-BMSC-ABs还能够促进血管新生,表现为CD31阳性细胞数量的增加(图4)。这些结果表明,BMSC-ABs通过将M0巨噬细胞重编程为M2表型,减少炎症浸润,从而发挥抗炎和促血管新生的双重作用,加速伤口愈合。

图4 PCL-BMSC-ABs对伤口愈合的影响(原文中Figure 6)
本研究首次揭示了BMSC-ABs通过靶向CCL-1基因,驱动M0巨噬细胞向M2表型转化,从而促进皮肤伤口愈合的机制。通过电纺丝技术制备的PCL纤维支架能够有效负载和释放凋亡囊泡,实现局部持续释放miR-21a-5p,调节炎症和血管新生,协同促进伤口愈合。该研究为开发针对炎症和抗炎免疫反应失衡相关疾病的新型治疗策略提供了理论依据和实验基础。
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304224001855
引用这篇文章:
Su X, Yang J, Xu Z, et al. Fibrous scaffolds loaded with BMSC-derived apoptotic vesicles promote wound healing by inducing macrophage polarization. Genes Dis. 2025;12(2):101388.


