Cell Death Differ 山东大学齐鲁医院杨建民/张文程教授团队揭示巨噬细胞JAML促进动脉粥样硬化进展的作用机制
时间:2025-04-02 12:08:49 热度:37.1℃ 作者:网络
动脉粥样硬化性心血管疾病(ASCVD)是全球死亡的主要原因之一,也是一个日益严峻的公共卫生挑战。研究表明,动脉粥样硬化是一种慢性炎症性疾病,由免疫细胞产生各种促炎细胞因子驱动。在动脉粥样硬化过程中,单核细胞与活化的内皮细胞结合,迁移到内膜下空间,并分化为巨噬细胞。与组织炎症相关的各种晶体,以及成孔毒素或细胞外ATP等多种物质,可促进巨噬细胞中NOD样受体家族核苷酸结合寡聚化结构域样受体3 (NOD-like receptor thermal protein domain associated protein 3, NLRP3)炎症小体的激活,促进驱动动脉粥样硬化进展的关键促炎细胞因子—白细胞介素-1β (IL-1β)的分泌。鉴于NLRP3炎症小体激活在动脉粥样硬化和相关血管炎症进展中的重要作用,阐明NLRP3炎症小体激活的分子机制意义重大。
连接粘附分子样蛋白(Junctional adhesion molecule-like protein, JAML)是一种I型跨膜糖蛋白,参与介导细胞间相互作用并与细胞内蛋白结合,从而激活下游信号通路。既往研究表明,JAML主要在中性粒细胞和单核/巨噬细胞中表达,并在各种刺激下表达上调。尽管JAML与包括糖尿病肾病在内的多种人类疾病有关,但其在动脉粥样硬化,特别是在巨噬细胞中调节动脉粥样硬化的作用尚不清楚。
2025年3月28日,山东大学齐鲁医院心内科、络病理论创新转化全国重点实验室杨建民教授和张文程教授团队在Cell Death and Differentiation在线发表了题为“Macrophage junctional adhesion molecule-like (JAML) protein promotes NLRP3 inflammasome activation in the development of atherosclerosis”的研究论文,阐述了巨噬细胞特异性敲除JAML抑制NLRP3炎症小体的激活以及下游炎症因子的释放从而延缓动脉粥样硬化进展的作用及其机制,这些发现可能为动脉粥样硬化提供一个新的预防和治疗靶点。

为了探索JAML在动脉粥样硬化发病和进展中的作用,研究人员首先重新分析了先前发表的人类颈动脉粥样硬化数据集的研究数据,发现人类动脉粥样硬化斑块中JAML表达显著上调。通过构建动脉粥样硬化小鼠模型,发现斑块中JAML的表达也显著增加,且主要在巨噬细胞中高表达。研究人员进一步检测了JAML在人外周血单核细胞(PBMCs)和人单核细胞源性巨噬细胞(HMDMs)中的表达水平,发现JAML在CAD患者的两种细胞类型中的表达均显著升高。
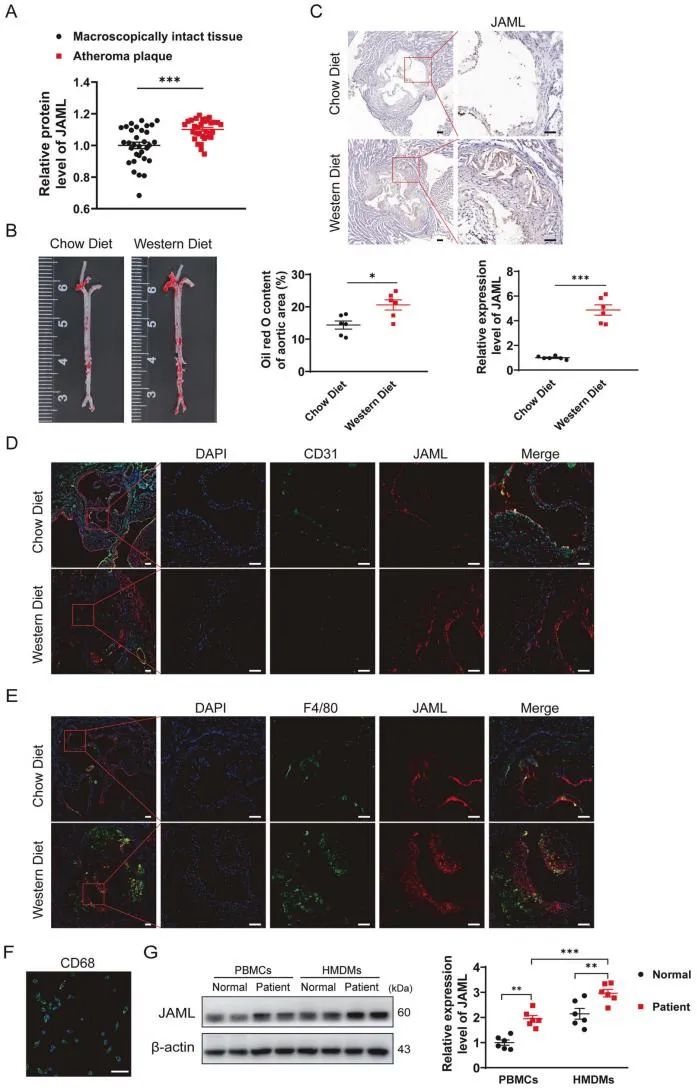
为探讨巨噬细胞中JAML在动脉粥样硬化中的作用,研究人员构建了巨噬细胞特异性敲除或过表达JAML小鼠并饲喂HFD饮食12周构建动脉粥样硬化小鼠模型。研究结果发现,巨噬细胞特异性敲除JAML能够延缓动脉粥样硬化的进展,减少脂质沉积和巨噬细胞浸润,而过表达JAML则加剧了上述现象。
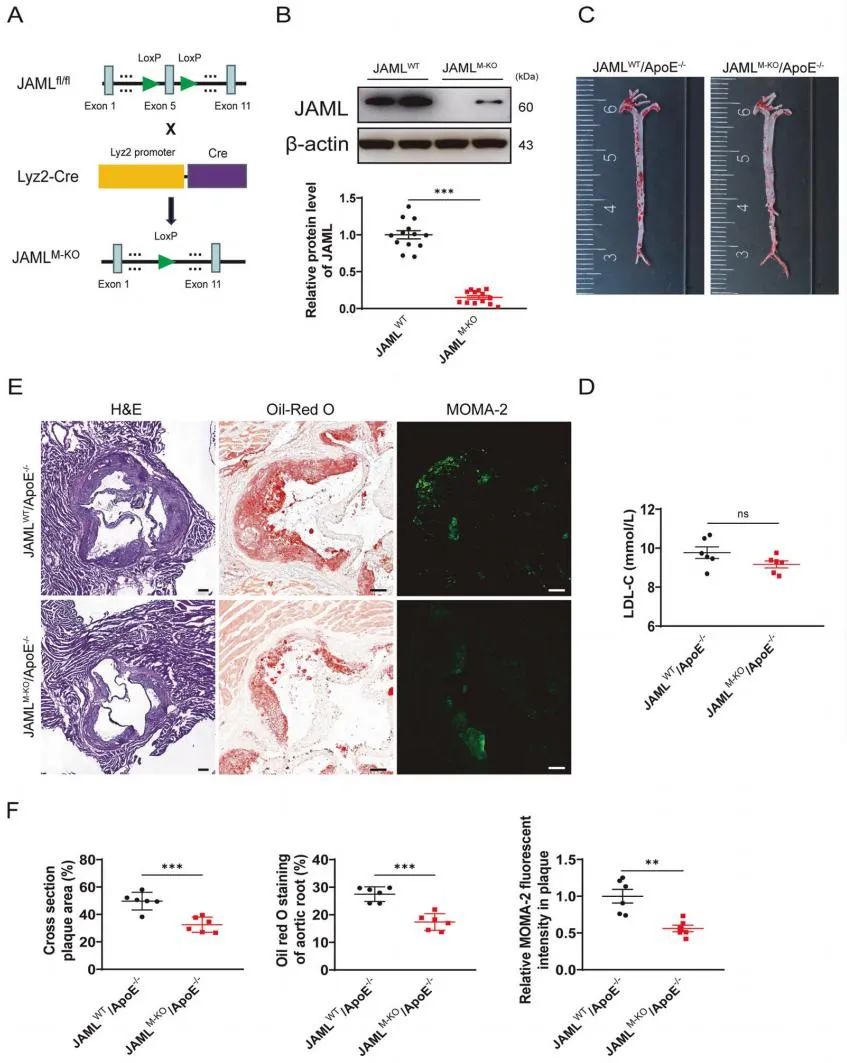
为进一步探讨JAML调控动脉粥样硬化的机制,研究人员在JAMLWT和JAMLM-KO小鼠中分离腹腔巨噬细胞进行转录组测序,发现两组间差异基因主要富集在NOD样受体信号通路。NLRP3炎症小体是由NLRP3、ASC和caspase-1组成的多蛋白复合物,介导caspase-1的激活,进而促进成熟的IL-1β和IL-18的释放。为了确定JAML是否影响NLRP3炎症小体的激活,研究人员在体内模型和细胞模型中对NLRP3炎症小体相关因子进行了检测,发现巨噬细胞中JAML的缺乏显著降低了NLRP3炎症小体的激活。
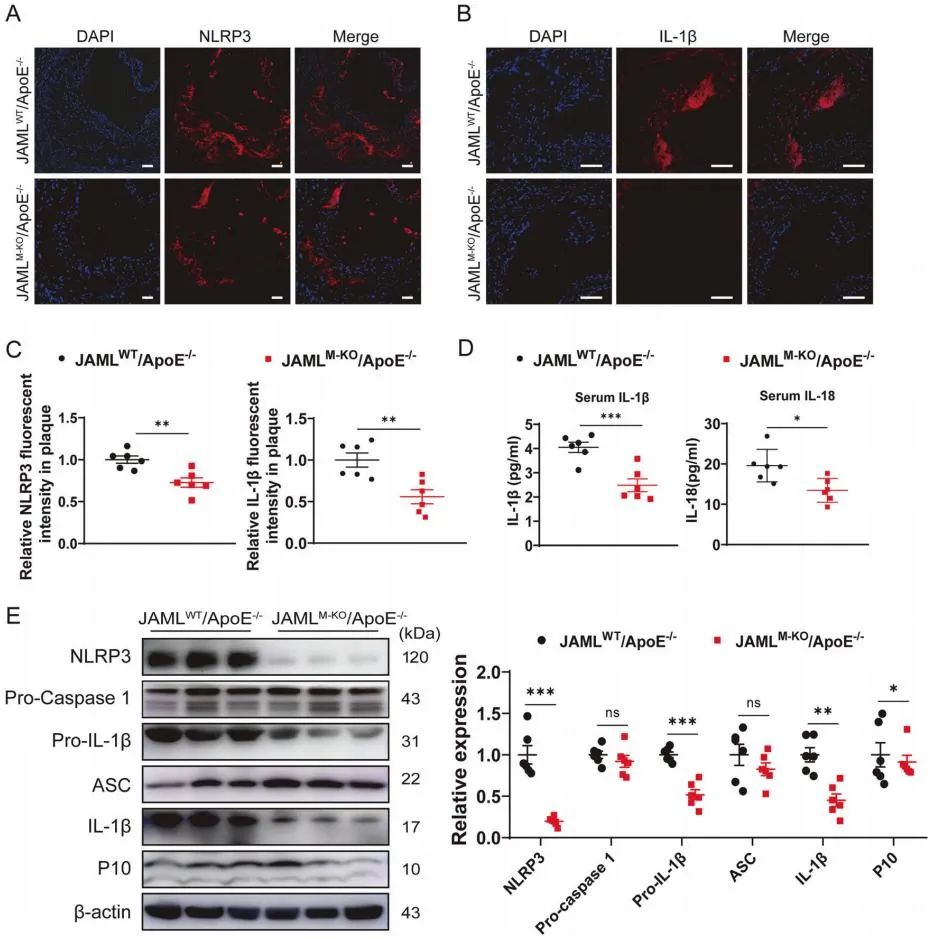
最后,研究人员探究了巨噬细胞中JAML调控NLRP3炎症小体激活的分子机制,发现JAML能够通过NF-κB途径促进NLRP3炎症小体的激活。通过质谱分析及免疫共沉淀证实,JAML的胞内结构域(ICD)与PKM2的A+B结构域存在相互作用。PKM2 Tyr105位点的磷酸化可阻止PKM2四聚体的形成,并促进非活性二聚体的形成,使其易位到细胞核并与NF-κB p65亚基结合。JAML缺乏不影响总PKM2蛋白表达,但显著降低p-PKM2水平、PKM2核易位以及PKM2与p65的结合,从而抑制NF-κB信号和NLRP3炎症小体的激活。这些结果表明,在巨噬细胞中,JAML通过与PKM2的相互作用调节NF-κB信号通路和NLRP3炎症小体的激活。
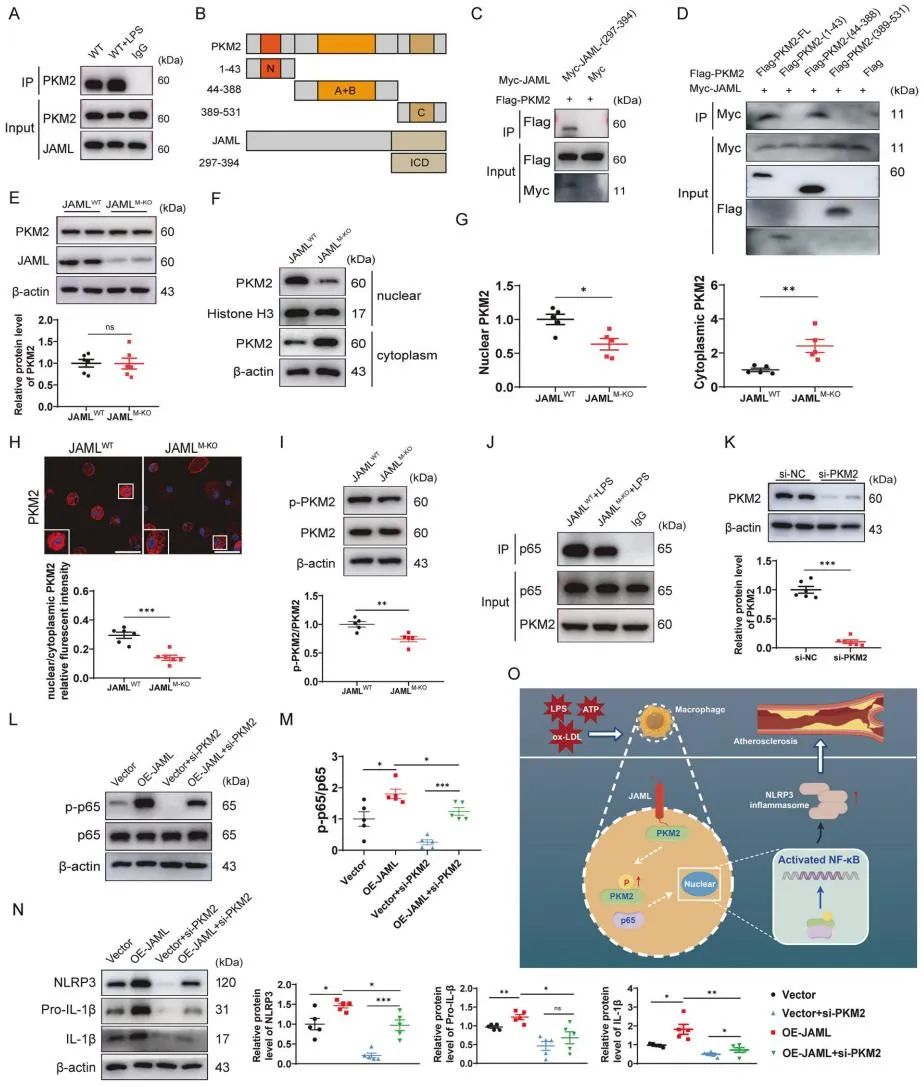
综上所述,该研究证实了在动脉粥样硬化小鼠斑块中巨噬细胞JAML的蛋白表达显著升高。JAML通过调节PKM2磷酸化和核易位激活NF-κB信号通路,导致NLRP3炎症小体激活,随后分泌促炎细胞因子,并最终加速动脉粥样硬化的进展。因此,巨噬细胞中JAML在调节NLRP3炎症小体激活和动脉粥样硬化进展中起着至关重要的作用,并为该疾病的抗炎治疗提供了潜在的靶点。
本论文的第一作者是山东大学齐鲁医院心内科博士研究生崔会良、博士后谢琳和博士后吕翰林,山东大学齐鲁医院心内科杨建民教授和张文程教授为该论文的共同通讯作者。山东大学齐鲁医院为第一和通讯作者单位。
原文链接:
https://www.nature.com/articles/s41418-025-01489-5#Fun


