北京化工大学侯毅/张沛森团队《ACS Nano》:基于“连环计”策略的高分辨肿瘤血管磁共振成像
时间:2024-09-10 19:01:53 热度:37.1℃ 作者:网络
肿瘤血管系统在肿瘤的发生、发展和转移过程中起到至关重要的作用,不仅为肿瘤细胞提供必需的营养和氧气,也成为肿瘤细胞扩散和转移的主要途径之一。因此,肿瘤血管的多样性被认为是肿瘤分级和预后的关键因素。但是到目前为止,肿瘤血管系统的综合评价仍然面临巨大的挑战,尤其是肿瘤血管系统的三维评价。鉴于此,北京化工大学侯毅、张沛森团队基于前期发展的高分辨血管磁共振血管造影(MRA)策略(Nat. Commun. 2023, 14, 6149;J. Mater. Chem. B 2020, 8, 6956-6963;Nanoscale Adv. 2023, 5, 3913),利用“连环”造影剂PAA-Gd,实现了实体肿瘤增长过程中肿瘤血管生成与演变过程的可视化检测,分析了其与肿瘤进展的关系,并研究了该策略在不同种类实体瘤的复杂微血管高分辨率可视化的可行性。相关工作以“High-Resolution Magnetic Resonance Angiography of Tumor Vasculatures with an Interlocking Contrast Agent”为题,发表在ACS Nano。

【文章要点】
一、“连环计”策略
“连环”造影剂PAA-Gd是将临床小分子造影剂Gd-DTPA链接到聚丙烯酸(PAA)的侧链上,可以有效规避单个小分子T1增强效果低、血液循环时间短的弊端。同时,由于PAA链段的限制以及 “兼性离子”结构,PAA-Gd造影剂能够有效滞留在血管内部,使得材料有很长的血液半衰期(69.2分钟),为获得三维肿瘤血管造影提供了延长的成像窗口。更重要的是,PAA-Gd具良好的生物相容性,能够满足注射计量的足够安全性,且在注射12小时后,95%以上的PAA-Gd可通过肝肾代谢(图1)。
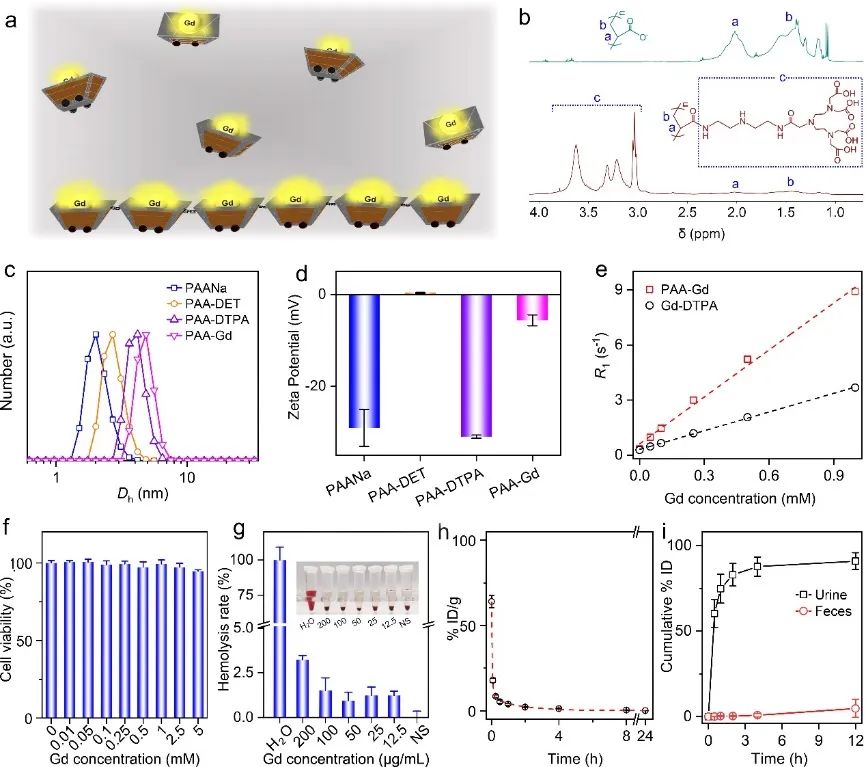
图1. “连环”造影剂的示意图及基本性质表征
二、实体瘤的复杂微血管高分辨率成像。
图2和图3展示了小鼠动态对比增强MRA图像。注射PAA-Gd后,血管结构清晰可见,注射临床小分子Gd-DTPA后,血管对比度低,血管细节无法显示。随后,在同一只4T1乳腺癌荷瘤小鼠模型中再次验证了PAA-Gd的高分辨率肿瘤血管可视化能力。进一步,将PAA-Gd应用到CT26结肠癌及Hepa1-6肝癌荷瘤小鼠模型,验证了该“连环”造影剂在不同类型肿瘤MRA诊断中的普适性。
在上述工作基础上,进一步对肿瘤血管生成与演变过程进行了研究。如图4三维肿瘤血管成像所示,随着肿瘤的发展,肿瘤组织及周围的主要血管及其分支增多、变粗。CD34免疫组化结果进一步表明,随着肿瘤的发展,微血管数量增加,血管管腔增大,血管壁增厚。定量分析表明,肿瘤体积和血管体积均随时间显著增加,而肿瘤内血管的密度随肿瘤增长先快速上升,然后保持稳定。
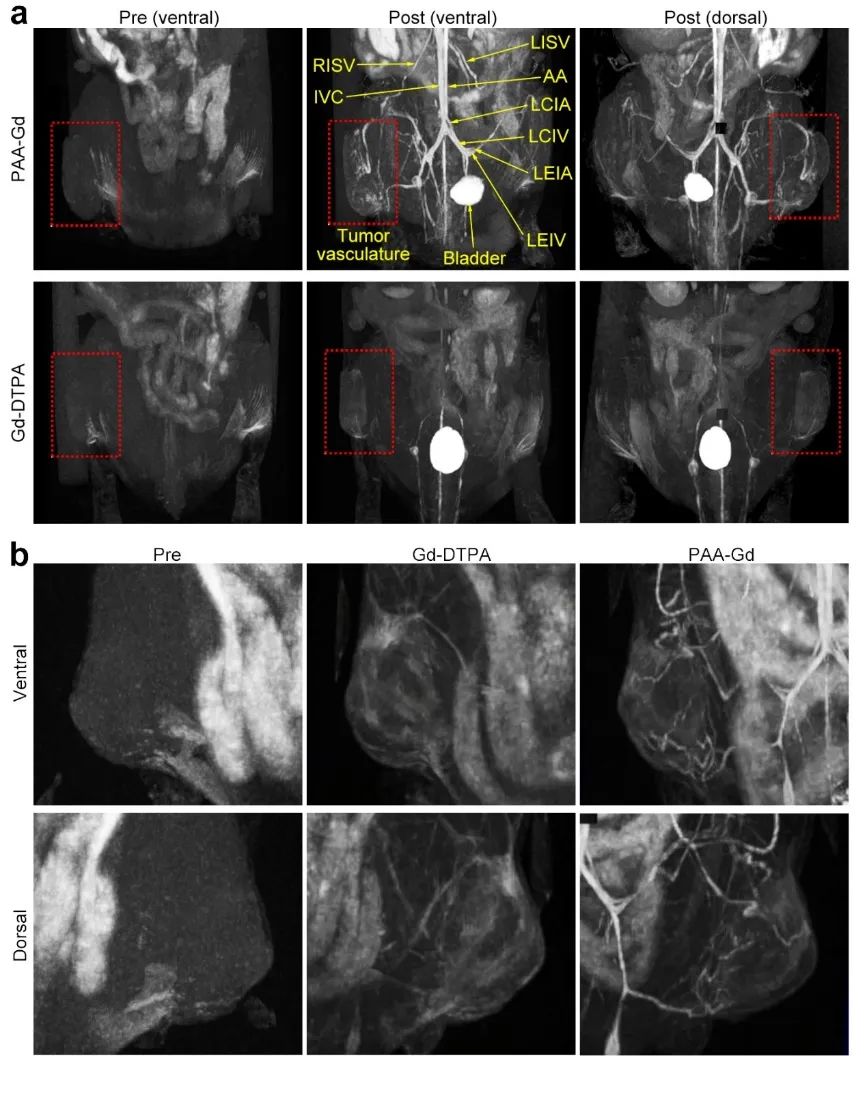
图2. 小鼠高分辨率三维动态对比增强(3D DCE)磁共振造影
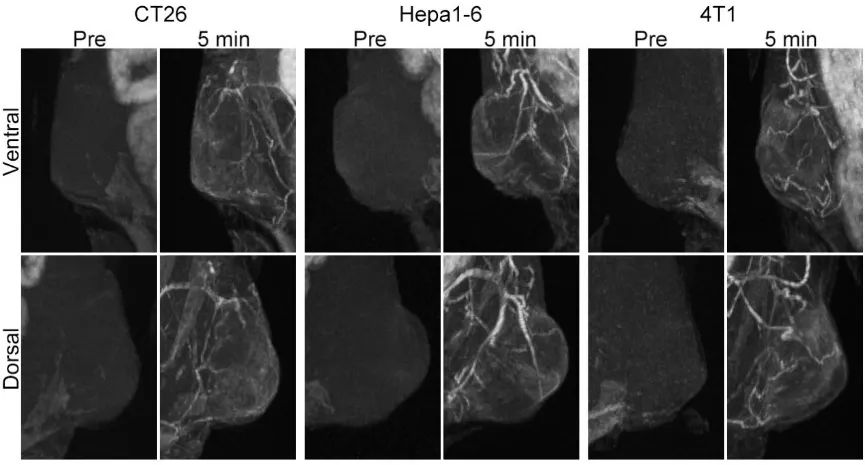
图3. CT26、Hepa 1-6及4T1小鼠荷瘤模型MRA影像
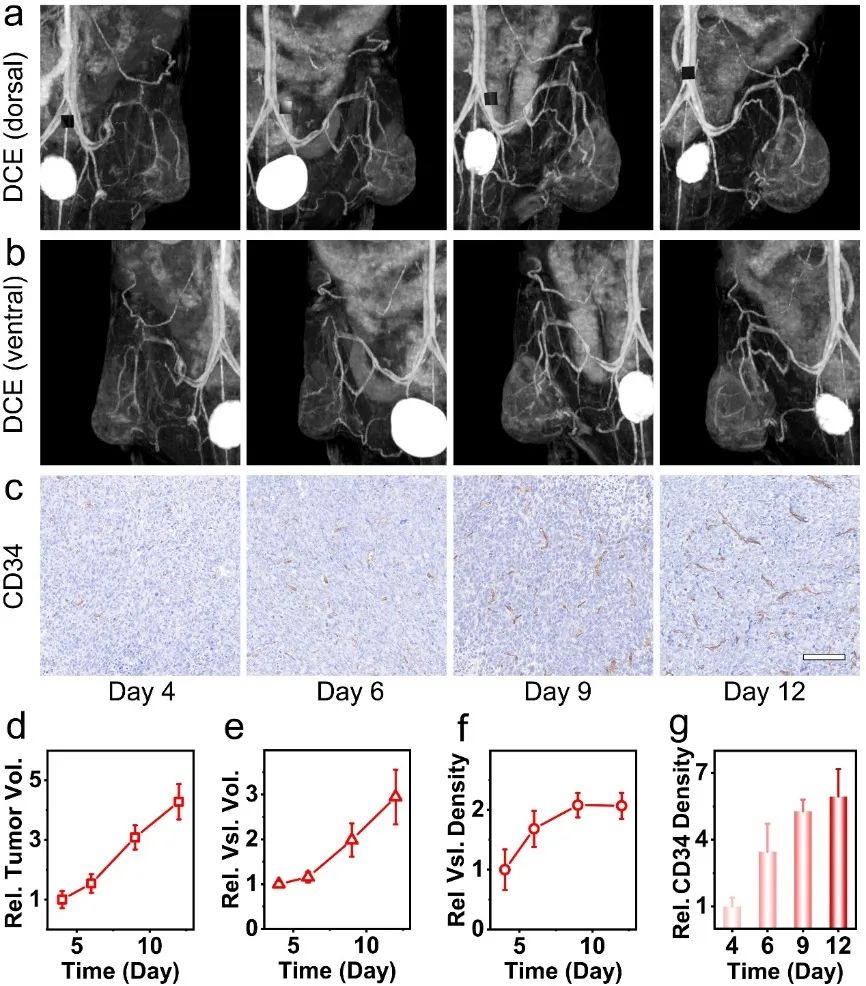
图4. PAA-Gd连续监测肿瘤血管生成
原文链接:
https://doi.org/10.1021/acsnano.4c07533


