靶向整合素的癌症治疗
时间:2024-09-03 23:00:32 热度:37.1℃ 作者:网络
前言
整合素是细胞粘附和信号蛋白,在各种广泛的生物学功能中起着非常重要的作用。目前,靶向整合素的药物已经在包括心血管疾病、炎症性肠病/多发性硬化症和干眼病等领域得到广泛开发。
然而,虽然整合素作为各种癌症的潜在治疗靶点已经研究了超过25年,靶向整合素的癌症药物仍未有突破。最近的研究强调了整合素治疗癌症的多个有希望的独立机制,整合素药物的设计现在可能处于一个转折点,有机会探索新的模式,并结合药理学和结构生物学的新发现,实现在肿瘤治疗的突破。
整合素的结构和功能
整合素蛋白是普遍存在的异二聚体跨膜糖蛋白受体,主要作为哺乳动物的信号蛋白。每个整合素由一个α-亚单位和一个β-亚单位组成,其中分别有18和8个变体,产生24个已知的异二聚体。α-和β-亚单位以在非共价结合方式形成复合物,形成表面的配体结合位点。
整合素作为粘附受体,具有跨膜针对两个方向发送信号的超常能力。它们要么与细胞外配体结合,要么通过整合素细胞内结构域与细胞骨架相互作用。因此,整合素可以使人类细胞对细胞外环境的变化作出反应(通过由外而内的信号),并可以影响细胞外环境本身(通过由内而外的信号)。
当配体与受体结合时,来自细胞外的信息在细胞内传递,导致细胞极性、细胞骨架结构、基因表达、细胞存活和增殖的变化。相反,细胞内激活剂如talin-1与β亚单位的细胞质尾部结合,引起构象变化,使整合素进入高亲和力状态,更容易与细胞外配体结合,从而促进细胞迁移和细胞外基质(ECM)组装和重塑。
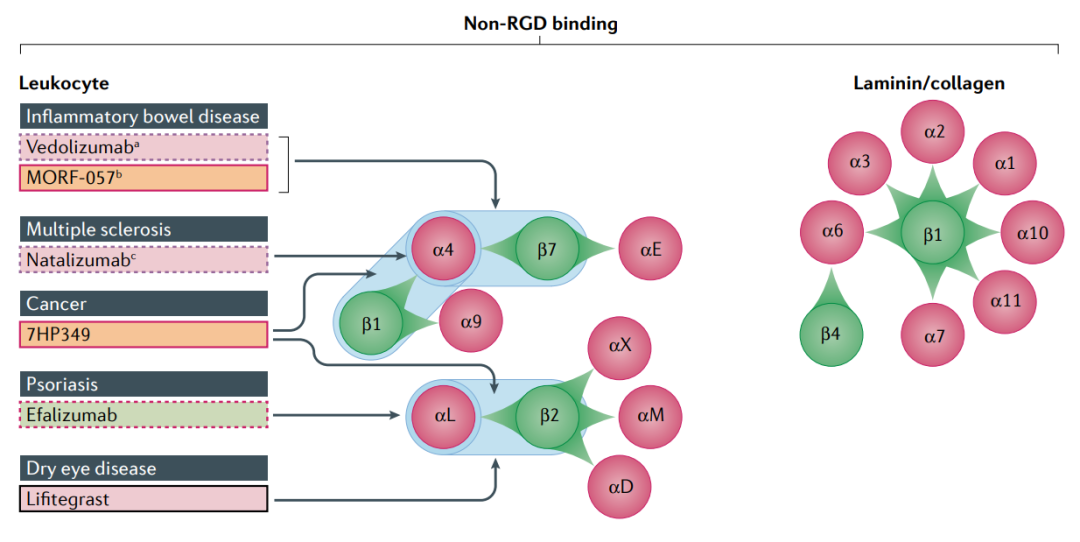
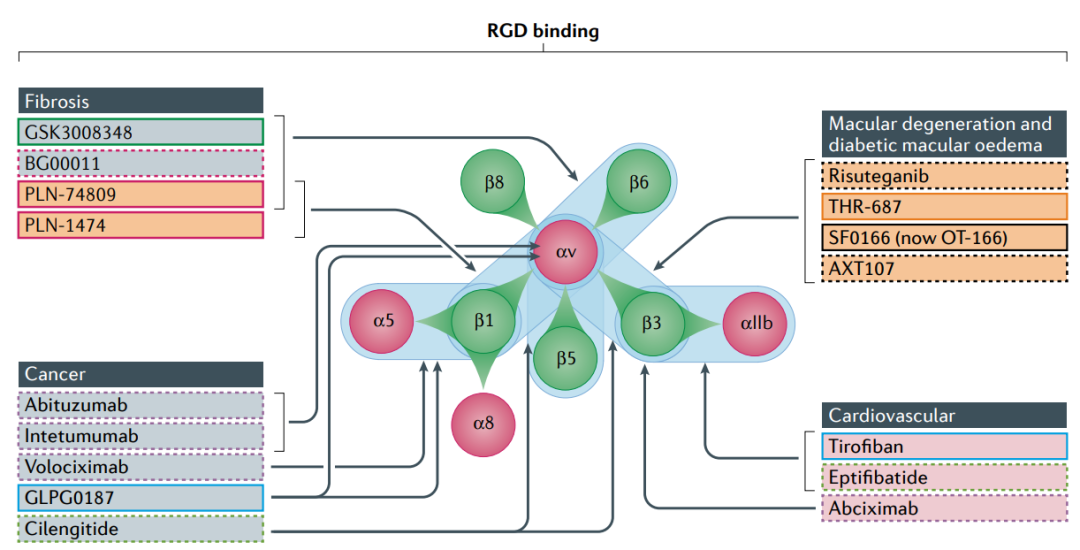
整合素蛋白分为由具有相关特性的受体组成的家族。例如,整合素RGD结合家族的所有八个成员都识别其内源性配体中的氨基酸结合基序Arg–Gly–Asp(RGD)。相关的整合素α4β7和α4β1是在白细胞上表达的治疗靶点。此外,与胶原蛋白或层粘连蛋白结合的整合素家族在疾病中具有广泛的作用。
靶向整合素的药物开发
整合素的抑制剂已经有几种上市药物,还有许多其他药物正在进行临床前研究。自2015年以来,至少有130项整合素靶向治疗的临床试验。总共有6种整合素抑制剂药物,针对四种整合素,包括αIIbβ3(也称为糖蛋白IIb/IIIa)、α4β7、α4β1和αLβ2。
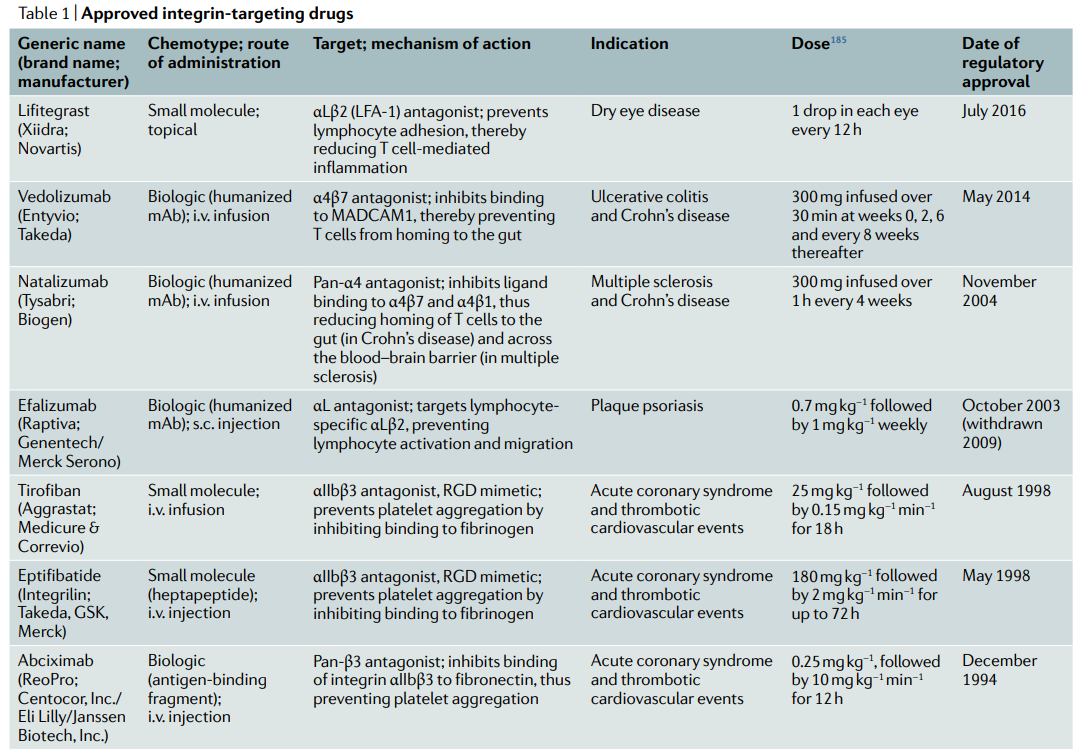
这些药物中有三种是抗体,三种是小分子。静脉给药的RGD结合整合素αIIbβ3抑制剂是最早开发的抑制剂之一,包括两种小分子tirofiban和eptifibatide以及抗体Abciximab,所有三种疗法均针对急性冠状动脉综合征和血栓性心血管事件。此外,以整合素αLβ2为靶点的药物有一种上市的小分子-lifitegrast,用于干眼症的局部治疗,αLβ2抑制剂也被研究用于自身免疫性疾病和炎症性疾病。
其余上市的整合素药物vedolizumab和natalizumab是主要作用于白细胞整合素α4β7和α4β1的抗体,用于治疗溃疡性结肠炎、克罗恩病和多发性硬化症。这两种分子的总销售额每年已超过40亿美元,突出了整合素抑制剂在治疗疾病方面的作用。然而,这类分子在2009年遭遇挫折,因为多个进行性多灶性白质脑病(PML)病例,靶向αL整合素的efalizumab退出市场。
目前,两种口服α4β7拮抗剂正在进行临床试验:一种来自Morphic Therapeutics的小分子(处于第一阶段)和一种来自ProtagentTherapeutics的肽(处于第二阶段)。
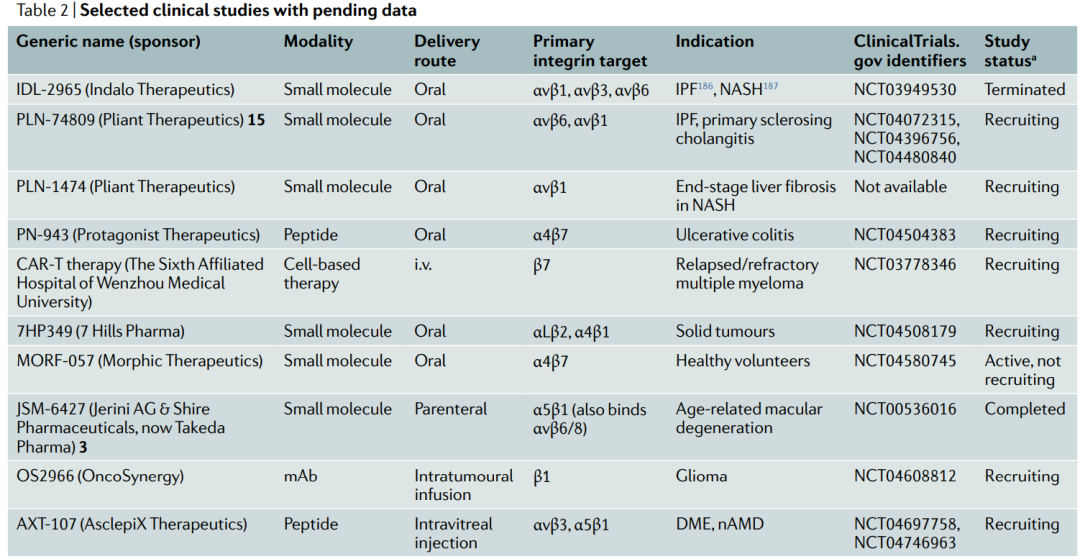
其它还有靶向含αv的整合素的新分子目前正在进入纤维性疾病的临床试验,包括特发性肺纤维化(IPF)和非酒精性脂肪肝炎(NASH),这些疾病有很高且不断增加的未满足的医疗需求。由于整合素蛋白是众多生物学途径的关键,并且它们与多种内源性配体结合,因此抑制单个整合素或整合素家族可治疗一系列疾病,如多种纤维性疾病或多种癌症。
靶向整合素的肿瘤药物开发
从历史上看,靶向整合素癌症药物的开发主要集中在RGD结合整合素家族,αvβ3仍然是过去二十年中研究最多的整合素。肿瘤靶向αvβ3的基本原理来自其在肿瘤血管生成中的已知作用及其对内皮细胞的上调,αvβ3抑制剂在临床前模型中具有积极作用,然而,这些研究并没有有效地转化为临床。
尽管靶向αvβ3整合素的分子通常具有可接受的安全性,但主要由于缺乏疗效,人们对使用它们治疗癌症的兴趣已经减弱。研究最多、进展最快的αvβ3抑制剂分子是环肽cilengitide(Merck KGaA),它也抑制αvβ5和α5β1,并已在大约30个不同的癌症临床试验中进行了评估。然而,最终,由于对胶质母细胞瘤缺乏疗效,cilengitide在III期试验中未能达到预期效果,总体生存率没有改善。针对αvβ3的抗体,如etaracizumab(MEDI-522;Abergrin)也进入了包括癌症在内的多种疾病的临床试验,但进展已经停止。GLPG0187是一种广谱αv抑制剂,尽管耐受性良好,但在实体瘤患者的Ib期试验中同样未能显示出疗效迹象。
虽然,已有的临床研究未能展示出临床疗效,然而最近的研究显示出整合素治疗癌症的三个有希望的独立机制:降低癌细胞中PD-L1的表达,降低肿瘤微环境中TGF-β的水平,以及靶向T细胞的整合素以增强细胞毒性和渗透能力。
整合素参与PD-L1表达的调节,因此是免疫逃避的重要组成部分。αvβ3在肿瘤微环境中积极调节PD-L1的表达,在小鼠研究中,αvβ3的缺失限制了原发肿瘤的生长。这一点尤其重要,因为大多数接受抗PD-1或抗PD-L1治疗的癌症患者对治疗没有反应,抗αvβ3治疗可能使肿瘤对该轴的破坏敏感,因此与PD-1或PD-L1靶向药物联合使用可能是有效的。
与αvβ3类似,阻断αvβ8可增强肿瘤中的细胞毒性T细胞反应。与αvβ3相比,肿瘤中的αvβ8表达通常与PD-L1表达无关。αvβ8通过与αvβ3不同的机制促进肿瘤的发生,该机制可能涉及TGF-β。在这种免疫逃避的替代机制中,活性TGF-β通过与肿瘤细胞或潜在免疫细胞上的αvβ8结合,从其存在于免疫细胞上的潜伏形式释放出来。肿瘤基质中的活性TGF-β可以阻止T细胞渗透到肿瘤中,从而保护肿瘤免受T细胞攻击。
αvβ6和成熟的靶点α4β7作为治疗靶点引起了广泛的兴趣。在过去5年中,一些新的αvβ6和/或αvβ1整合素抑制剂(大部分为小分子)已进入临床试验阶段,α4β7定向疗法(大部分为抗体)已进入后期临床试验阶段。焦点从αvβ3到αvβ6的变化也将下游效应器途径的焦点从血管生成转移到调节或抑制TGF-β途径。临床试验研究了泛αv抗体abituzumab和intetumumab分别作为单一疗法、或联合化疗和EGFR抑制剂治疗结直肠癌和黑色素瘤的疗效。尽管这两组研究在其主要终点均未取得统计学上显著差异,但有一些证据表明αvβ6高水平表达的结直肠癌患者的疗效有所改善。
此外,通过靶向整合素来改善T细胞粘附和活化也是一种作用机制。小分子7HP349对T细胞中白细胞特异性整合素αLβ2和α4β1的变构激活增强了T细胞的激活和粘附,从而改善了黑色素瘤和结肠癌小鼠模型中T细胞对肿瘤的渗透。该化合物目前处于第一阶段试验。
肿瘤上几种整合素的水平增加,通过靶向这些整合素可能是特异性靶向肿瘤细胞的有效策略。这种新方法不是直接抑制整合素,而是利用病变组织中的高局部表达。到目前为止,人们的工作主要集中在RGD结合方法上,将药物结合物靶向输送至肿瘤,SGN-B6A是一种整合素靶向的ADC药物,该药物可以识别β6以选择性靶向实体肿瘤,正处于1期临床试验(NCT04389632)阶段。
小结
尽管整合素作为肿瘤药物开发的靶点经历过一些挫折,但基于最近对于整合素新机制的认识,人们对其作为肿瘤药物靶点重新产生了兴趣。为了取得成功,目前的整合素项目应该注意到已经完成的许多整合素靶向试验的关键经验教训,未来以整合素为目标的计划应侧重于开发能够充分测试机制的分子,稳健的目标验证,衡量目标参与度的临床研究,以及开发生物标志物来衡量临床疗效。有了这些变化,相信整合素作为靶点将在肿瘤治疗上拥有一席之地。
参考文献:
1.Emerging therapeutic opportunities forintegrin inhibitors. Nat Rev Drug Discov. 2021 Sep 17 : 1–19.


