把握早期治疗窗口,规范用药提升疗效--甲氨蝶呤在类风湿性关节炎治疗中的研究进展
时间:2024-08-15 10:01:02 热度:37.1℃ 作者:网络
2024年8月8日中华医学会第二十七次风湿病学学术会议在湖北武汉召开。这是我国年度规模最大、学术水平最高的风湿病学学术会议,聚集了国内权威专家,吸引了来自全国各地5000多名风湿领域的专家学者参与。会议共设188场学术盛宴,包含2场主题演讲、101场专题报告、3场研讨会、31个专题会议、8场专家面对面交流和43场论文报告,内容涵盖了风湿免疫病及其相关的临床与基础研究、新技术与新科技的发展以及未来趋势,会议以“变革”为主题,深刻揭示了医学领域当前所面临的机遇与挑战,为促进风湿病学科的发展与健康服务提供了重要的平台和机会。 

8月9日,在恩施慧宜中西医结合风湿医院向阳教授主持下,山西医科大学第二医院王彩虹教授以“牢握机会之窗,及早规范治疗--甲氨蝶呤在类风湿关节炎治疗中的研究进展”为题作精彩分享,特别对甲氨蝶呤在类风湿性关节炎的规范化治疗进行剖析。




免疫介导炎症性疾病
未来从预防到治愈是发展趋势
王彩虹教授带领大家回顾了免疫系统在感染与免疫介导疾病过程中的关键作用。她详细讲解了CD4+T细胞、CD8+T细胞、巨噬细胞和浆细胞的功能,强调了免疫失调可能引发的疾病,如自身免疫病和癌症。她指出,炎症反应虽然在免疫过程中至关重要,但过度炎症会导致组织损伤和病情加重。特别是在类风湿性关节炎等炎症介导疾病中,早期诊断和治疗对于遏制疾病进展、减轻患者痛苦和组织损伤至关重要。她呼吁加强对免疫状态的关注,以改善患者的健康和生活质量。
早诊早治疗,
类风湿关节炎治疗刻不容缓
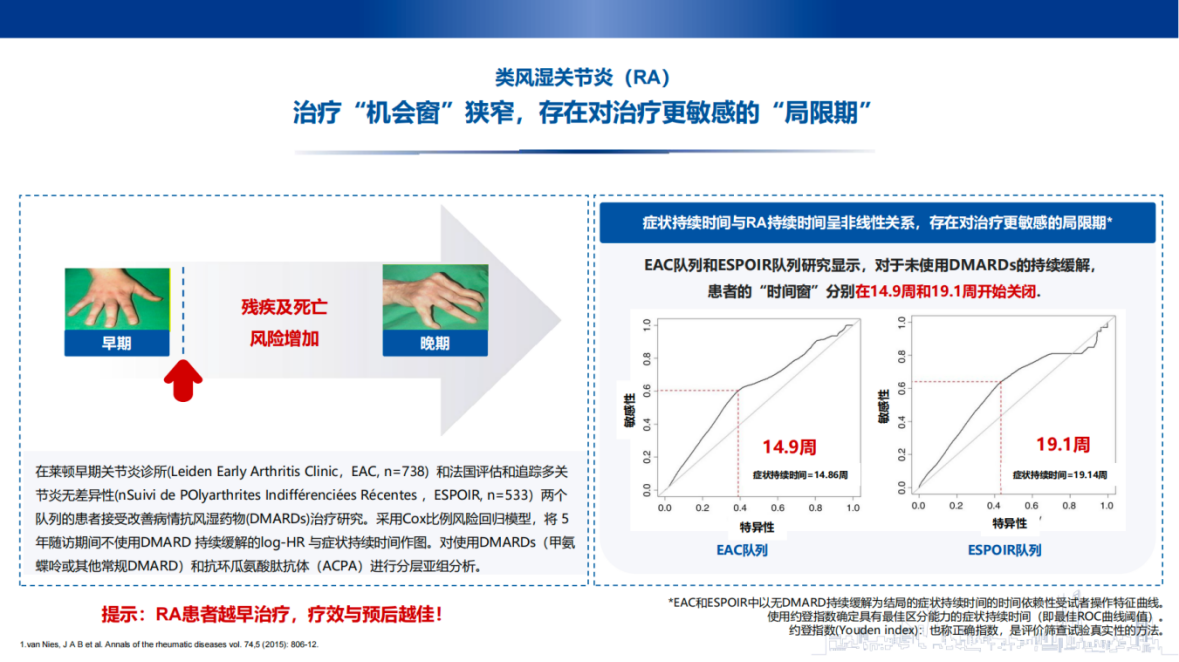
类风湿关节炎(RA)随着病程的延长,其残疾和功能受限的发生率显著上升。RA不仅导致患者身体机能下降、生活质量降低和社会参与度减弱,同时也给患者家庭和社会带来了巨大的经济负担。研究显示,RA患者在病程达到10-15年时的致残率高达61.3%,远高于病程不足10年的患者1。
RA的治疗存在一个狭窄的“机会窗”,其中包含一个对治疗更为敏感的“局限期”。莱顿早期关节炎诊所(Leiden Early Arthritis Clinic, EAC, n=738)和法国ESPOIR队列(n=533)的研究结果表明,对于未使用疾病修饰抗风湿药物(DMARDs)的患者,其“机会窗”在14.9周(EAC队列)和19.1周(ESPOIR队列)时开始关闭2。
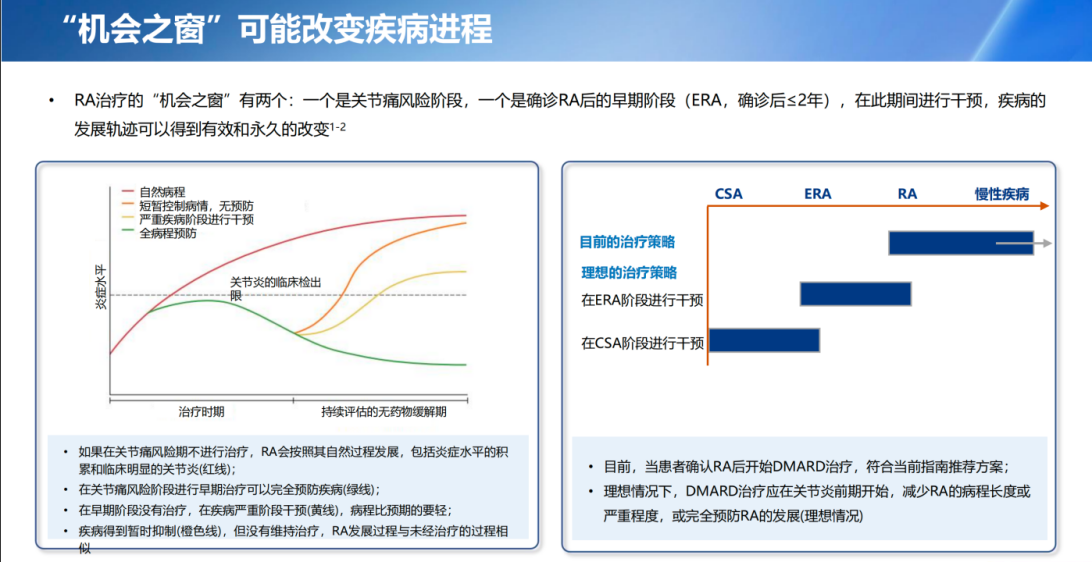
RA的发生和发展过程揭示了潜在的预防机会。早期干预可能有效地预防疾病的进展3。RA治疗的“机会窗”包括两个关键阶段:一个是关节疼痛的风险阶段,另一个是确诊RA后的早期阶段(ERA,确诊后≤2年)4。在这两个阶段进行干预,可能有效且永久地改变疾病的发展轨迹。理想情况下,DMARD治疗应在关节炎前期开始,减少RA的病程长度或严重程度,或完全预防RA的发展(理想情况)。
尽管新的疗法不断出现,RA的初始治疗仍以低剂量甲氨蝶呤(MTX)为主。在部分患者中,单独使用甲氨蝶呤(MTX)即可显著改善病情;对于对MTX反应不足的患者,则需要联合使用生物制剂或Janus激酶(JAK)抑制剂等药物3。MTX与多种靶向药物的联合使用能够进一步增强临床反应效果。早期干预不仅在预防RA方面至关重要,还凸显了确定长期RA新靶点以及制定新的分类标准的必要性3。此外,研究表明,MTX和阿巴西普的治疗均能降低亚临床关节炎的炎症水平,尤其是MTX在改善亚临床关节炎的严重程度、症状、残疾以及工作能力方面具有持久的影响4。这些益处不仅限于自身抗体阳性或确诊为RA的患者,对自身抗体阴性患者及尚未发展为RA的患者同样有益。PROMPT研究验证了MTX在治疗疑似RA患者中的有效性,并且能够延缓疾病进展5。中国类风湿关节炎诊疗指南(2018)及EULAR(欧洲抗风湿病联盟) 2022年类风湿关节炎治疗建议均推荐甲氨蝶呤作为RA治疗的一线首选药物。
生物制剂与甲氨蝶呤联用,
可提高生物制剂疗效与安全性
多项研究验证了生物制剂单药治疗与甲氨蝶呤(MTX)单药治疗相比,在疗效上未见显著优势。例如,在TEMPO研究中,依那西普(Etanercept)单药治疗与MTX相比,疗效无显著差异。然而,两者的联合治疗显著提高了ACR反应率,并且DAS评分也明显改善6。依那西普联合MTX在3年内表现出持续的疗效,并且其效果优于任何一种单药治疗6。
TEMPO研究
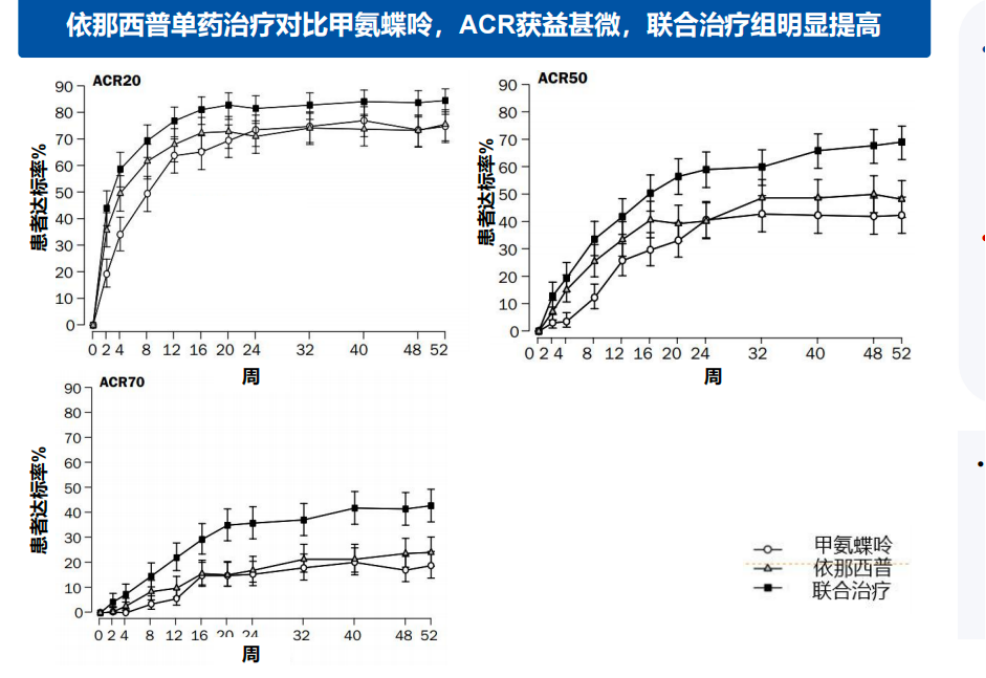
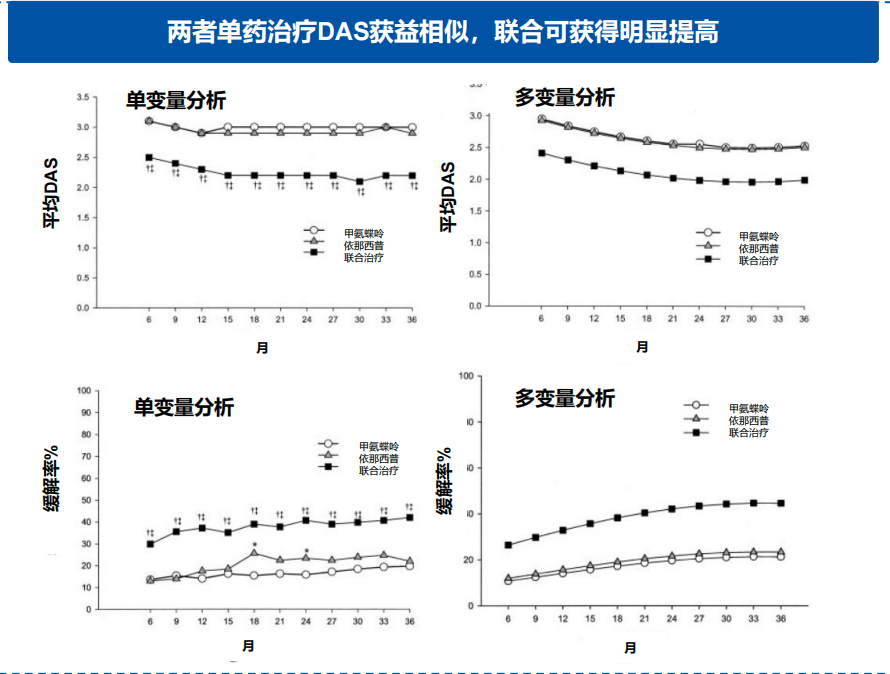
此外,PREMIER研究发现,阿达木单抗(Adalimumab)单药治疗在第1年和第2年的ACR50反应率方面与MTX无显著差异,但在所有评估指标中,联合治疗均优于单药治疗7。
PREMIER研究
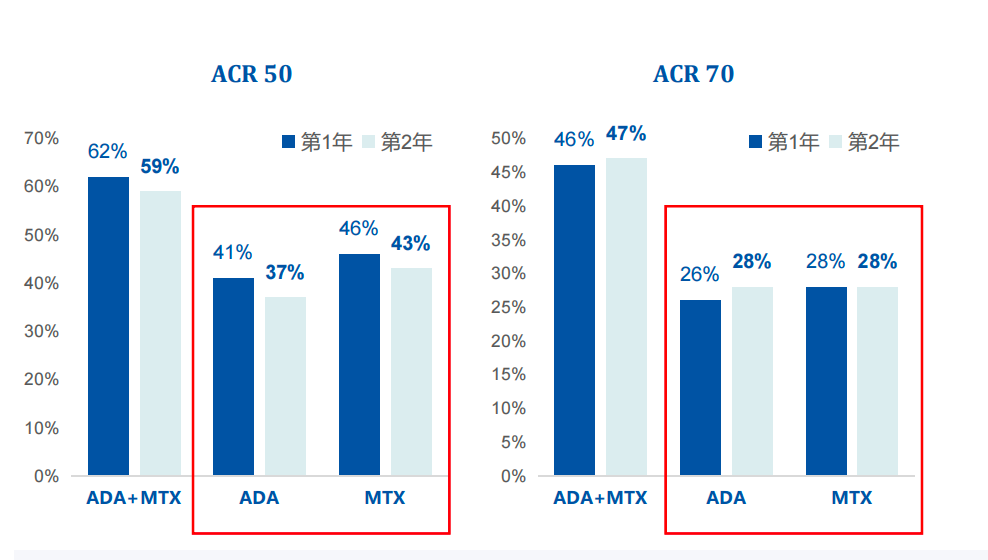
AMBITION研究表明,托珠单抗(Tocilizumab)单药治疗虽有疗效,但与MTX相比,显示出更高的不良反应发生率,如中性粒细胞减少和胆固醇升高8。
AMBITION研究
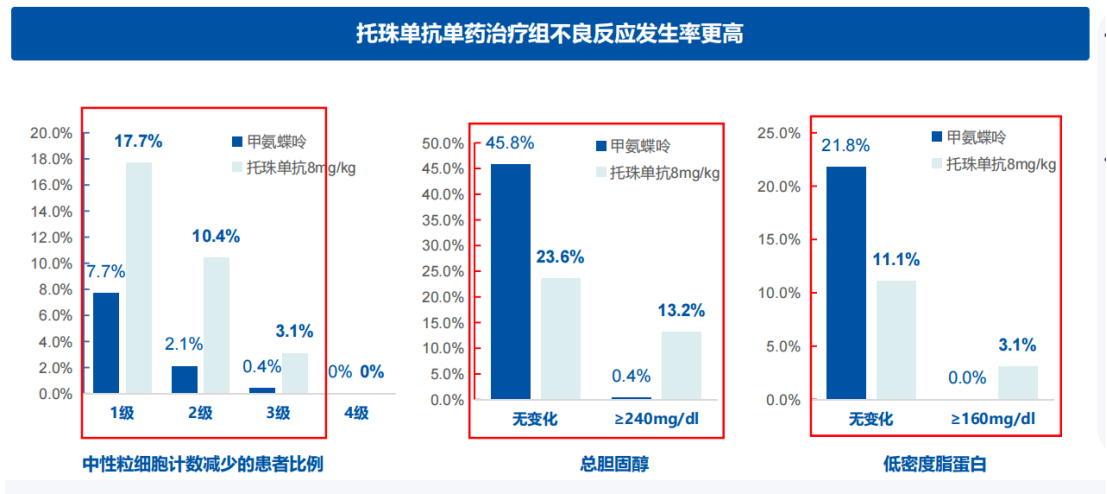
系统性评价也进一步表明,TNF抑制剂如阿达木单抗与MTX联合治疗时,其EULAR反应优于与其他csDMARDs联合使用,且联合治疗可降低抗药抗体的产生9。

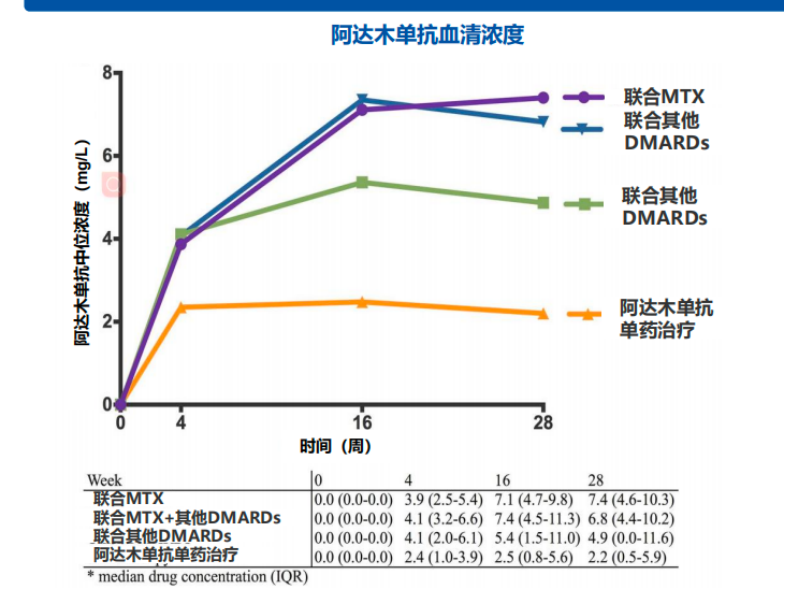
此外,甲氨蝶呤不仅在抗炎效应上具有优势,还可能降低心血管疾病风险,并延缓类风湿关节炎相关间质性肺病(RA-ILD)的发作10。
综上所述,尽管生物制剂单药治疗在某些情况下显示出一定疗效,但其与MTX联合使用能更显著地改善治疗效果,且联合治疗方案在临床上更具优势。根据中国类风湿关节炎诊疗指南,对于初始治疗后未达到预期疗效的患者,建议采用联合用药方案。在这种方案中,甲氨蝶呤是csDMARDs与bDMARDs或tsDMARDs联合用药的首选药物。研究表明,甲氨蝶呤与bDMARDs或tsDMARDs联合使用,疗效显著优于单药治疗11。甲氨蝶呤作为csDMARDs中的基础药物,与生物制剂或JAK抑制剂的联合应用,不仅提升了疗效,也在一定程度上优化了治疗的安全性和可接受性。
预充式甲氨蝶呤RA适应症获批,
中国唯一一个拥有RA适应症的甲氨蝶呤制剂
在类风湿关节炎的治疗领域,优化甲氨蝶呤的应用一直备受关注。皮下注射甲氨蝶呤因其良好的生物利用度和药效学特性,成为初始治疗或口服治疗失败后的重要考虑。研究表明,初始使用皮下注射甲氨蝶呤或从口服转为皮下注射,可显著提高治疗的持久性和疗效。对于因不耐受或疗效不佳而口服甲氨蝶呤治疗失败的患者,转为皮下注射甲氨蝶呤(SC MTX)是一个有效的“挽救”措施。数据显示,70%至80%接受口服甲氨蝶呤单药治疗的患者未能达到低疾病活动度,改用皮下注射后,疗效得以显著提升12。
皮下注射甲氨蝶呤通过突破口服给药的浓度限制,稳步提高药物的生物利用度,尤其是在剂量≥15mg/周时,药物在体内的全身浓度稳步上升13。对于对口服甲氨蝶呤反应不足的患者,改用皮下注射形式可以从更高的药物暴露浓度中获益。与传统治疗方案相比,皮下注射甲氨蝶呤的疗效(如DAS28-CRP评分)得到显著提高,同时安全性方面未见明显副作用的增加14。最新的循证医学证据也支持皮下注射甲氨蝶呤的广泛应用。值得注意的是,预充式甲氨蝶呤注射液(美泰彤®)已在中国获批用于治疗类风湿关节炎,成为中国唯一获得此适应症的甲氨蝶呤制剂。

在此次会议中,多位专家学者深入探讨了甲氨蝶呤在类风湿关节炎(RA)治疗中的作用。专家们指出,虽然生物制剂在RA治疗中具有重要作用,但它们并未完全取代传统DMARDs药物。生物制剂通常在传统DMARDs疗效不足时,作为替代或联合治疗的选项被考虑。此外,有专家提出,对于合并多种并发症的RA患者或老年RA患者,预充式甲氨蝶呤注射液可能是更为适宜的治疗方案。
小结
甲氨蝶呤是RA治疗的一线首选药物,特别是在传统口服治疗失败或疗效不足的情况下,皮下注射甲氨蝶呤显示出更高的生物利用度和疗效。联合使用甲氨蝶呤与生物制剂或JAK抑制剂,可以显著改善患者的治疗效果并优化安全性。在多种并发症的患者中,预充式甲氨蝶呤注射液被认为是更为适宜的选择。


参考文献:
1.耿研,谢希,王昱,等.类风湿关节炎诊疗规范[J].中华内科杂志, 2022, 61(1):9.DOI:10.3760/cma.j.cn112138-20210616-00426.
2.Nagy, György et al. Annals of the rheumatic diseases vol. 80,1 (2021): 31-35.
3.. Gravallese EM, et al. N Engl J Med. 2023 Feb 9;388(6):529-542
4.van Steenbergen HW, et al. Nat Rev Rheumatol. 2023 Dec;19(12):767-777.
5.van Dongen, Henrike et al. Arthritis and rheumatism vol. 56,5 (2007): 1424-32.
6.中华医学会风湿病学分会. 2018中国类风湿关节炎诊疗指南[J]. 中华内科杂志,2018,57(4):242-251.
7.Klareskog, Lars et al. Lancet vol. 363,9410 (2004): 675-81.
8.Breedveld, Ferdinand C et al. Arthritis and rheumatism vol. 54,1 (2006): 26-37.
9.Decarriere, Guillaume et al. Arthritis care & research vol. 73,6 (2021): 873-884.
10.Pouw, Mieke F et al. Annals of the rheumatic diseases vol. 74,3 (2015): 513-8. doi: 10.1136/annrheumdis-2013-204172
11.Vogelzang, E H et al. Annals of the rheumatic diseases vol. 74,2 (2015): 474-5.
12.Detert, Jacqueline et al. Annals of the rheumatic diseases vol. 72,6 (2013): 844-50. doi:10.1136/annrheumdis-2012-201612
13.Kiely, Patrick et al. BMJ open vol. 9,5 e028466. 5 May. 2019
14.Bello, Alfonso E et al. Open access rheumatology vol. 9 67-79. 31 Mar. 2017


