Bone Res:中南大学胡建中/曹勇/吕红斌合作发现Kdm6a-CNN1轴在脊髓损伤中的作用机制
时间:2024-08-04 06:01:18 热度:37.1℃ 作者:网络
细胞衰老通过分泌促炎因子在各种疾病中发挥关键作用。尽管对与衰老和退行性疾病相关的血管衰老进行了广泛的研究,但创伤应激引起的微血管内皮细胞衰老的分子机制,特别是其在衰老诱导的炎症中的作用,仍未得到充分阐明。
2024年3月25日,中南大学胡建中、曹勇、吕红斌共同通讯在Bone Research 在线发表题为“Kdm6a-CNN1 axis orchestrates epigenetic control of trauma-induced spinal cord microvascular endothelial cell senescence to balance neuroinflammation for improved neurological repair”的研究论文,该研究中全面展示和描述了脊髓损伤(SCI)引起的微血管内皮细胞衰老。
赖氨酸脱甲基酶6A(Kdm6a),通常称为UTX,是受损脊髓微血管内皮细胞(SCMEC)中细胞衰老的关键调节因子。UTX的上调会诱导SCMEC中的衰老,导致促炎因子的释放增加,特别是衰老相关分泌表型(SASP)成分,从而调节炎症微环境。相反,内皮细胞中UTX的缺失可保护SCMEC免于衰老,减轻促炎性SASP因子的释放,并促进SCI后的神经功能恢复。UTX通过与钙调蛋白1(CNN1)结合形成表观遗传调控轴,协调创伤引起的SCMEC衰老和SASP分泌,从而影响神经炎症和神经功能修复。此外,局部输送抗衰老药物可减少衰老的SCMEC并抑制促炎性SASP分泌,恢复局部再生微环境并增强SCI后的功能修复。总之,针对UTX-CNN1表观遗传轴来预防创伤引起的SCMEC衰老具有抑制SASP分泌、减轻神经炎症并为SCI修复提供一种新的治疗策略的潜力。

脊髓损伤(SCI)是一种严重的中枢神经系统(CNS)创伤性疾病,通常会导致不可逆转的运动和感觉功能丧失。SCI的影响超出了身体范围,严重影响了患者的生活质量,常常导致残疾,对他们的整体健康构成风险。SCI带来的经济负担是巨大的,给受影响的家庭和更广泛的社会医疗保健系统带来了相当大的经济压力。SCI后,受损细胞会发生形态、生理、化学和免疫系统的改变,从而阻碍再生。SCI干预的临床策略主要包括早期手术减压、大剂量糖皮质激素给药、抗炎治疗和神经康复训练。尽管做出了这些努力,但仍然缺乏有效的治疗方式来促进受伤脊髓的恢复和再生。
尽管在揭示哺乳动物脊髓损伤(SCI)后的分子复杂性方面取得了重大进展,但治疗突破仍然难以实现。这种差异表明,对脊髓损伤后发生的病理改变的全面了解仍不完整。脊髓损伤后,血脊髓屏障(BSCB)立即破裂,促进免疫细胞外渗,从而形成促炎环境。脊髓损伤进一步被描述为由浸润巨噬细胞和活化星形胶质细胞驱动的炎症状态。炎症是衰老进化保守的机制基础之一。许多与年龄有关的疾病都表现出衰老细胞的积累。尽管衰老细胞具有非增殖性质,但它们具有影响微环境的能力,通过产生炎症介质与炎症状态建立密切的相关性。
然而,在创伤性中枢神经系统(CNS)疾病中,细胞衰老经常被忽视。内皮细胞在与其他细胞(包括周细胞、星形胶质细胞、少突胶质细胞、神经元等)的功能相互作用中起着至关重要的作用,有助于神经血管单元(NVU)的形成和中枢神经系统功能的正常维持。内皮细胞构建了供给中枢神经系统的血管网络,具有对维持体内平衡和促进神经功能修复至关重要的特殊结构。据报道,在退行性和衰老疾病中,血管内皮细胞会发生衰老。衰老内皮细胞中紧密连接的破坏导致血管通透性增加和正常血管功能受损。然而,血管内皮细胞是否在脊髓损伤(SCI)的创伤性病理生理过程中发生细胞衰老,以及衰老细胞是否分泌影响神经功能修复的促炎性衰老相关分泌表型(SASP)因子值得进一步探索。
创伤引起脊髓损伤微血管内皮细胞衰老(图源自Bone Research )
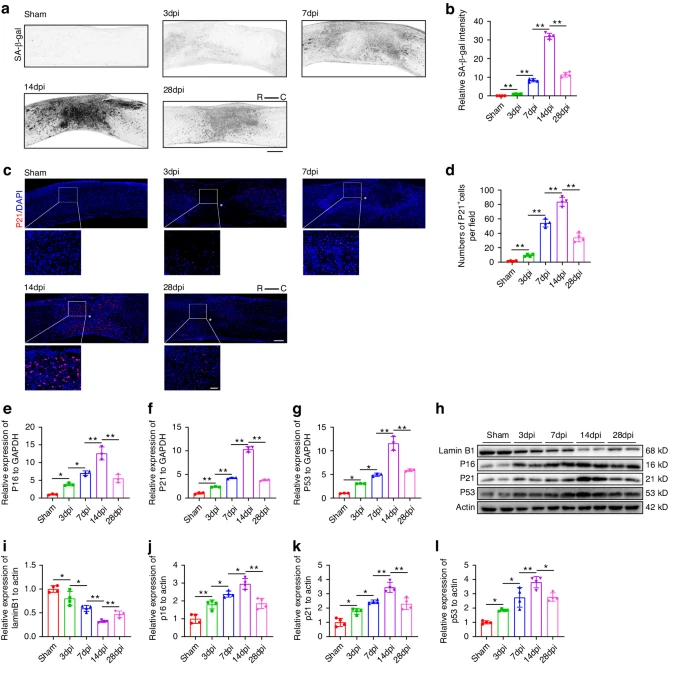
衰老细胞通常表达多种衰老生物标志物,包括P53、P21、P16、衰老相关β-半乳糖苷酶(SA-β-Gal)。衰老细胞的一个重要特征是SASP,它涉及多种细胞外调节剂的释放,包括细胞因子、趋化因子、生长因子和蛋白酶。通过释放SASP因子,衰老可以调节局部微环境并影响邻近细胞。值得注意的是,由不同应激刺激引起的衰老细胞可能表现出不同的SASP成分。越来越多的证据表明,表观遗传失调是细胞衰老的重要驱动因素,起着至关重要的作用。表观遗传修饰,包括染色质重塑、DNA甲基化和组蛋白改变,能够激活或抑制细胞衰老以响应各种刺激。衰老中表观遗传变化的多样性使得无法确定衰老细胞的通用表型。
据报道,组蛋白去乙酰化酶1/2(Hdac1/2)可维持正常的肾小球滤过功能。特定的Hdac1/2缺失可诱导足细胞衰老,产生大量的SASP和促炎细胞因子来损伤足细胞,最终导致蛋白尿增加和进行性肾衰竭。组蛋白甲基化酶Ezh2被发现通过靶向H3K27me3刺激Foxo1表达。该过程导致骨髓基质细胞(BMSCs)的抗氧化潜力降低,并导致BMSCs衰老。赖氨酸脱甲基酶6A(KDM6A),也称为X染色体上普遍转录的四肽重复序列(UTX),已被证明通过特异性去除H3K27上的二甲基和三甲基标记来调节非创伤性疾病中的细胞衰老。UTX通过脱甲基酶依赖性和非依赖性机制在调节造血系统中与衰老相关的基因中起着至关重要的作用。强烈建议探索调节创伤引起的内皮细胞衰老的典型表观遗传因素以及衰老细胞在受伤脊髓中诱导神经炎症特征的机制。
已证明,受伤脊髓中持续衰老的积累对功能修复有害。衰老清除疗法已在临床前小鼠实验中证明有效,它能消除衰老细胞,从而延缓、预防或缓解各种与年龄和衰老相关的疾病。已测试的衰老清除药物包括达沙替尼(D,FDA批准的酪氨酸激酶抑制剂)、槲皮素(Q,存在于许多水果和蔬菜中的类黄酮)、A1155463(Bcl-2促存活家族抑制剂)和非瑟酮(F,类黄酮)。达沙替尼和槲皮素(D + Q)代表第一代抗衰老药物,已在临床前衰老模型和各种疾病(包括骨骼、肌肉和神经系统疾病)中进行研究。
在肥胖小鼠中,达沙替尼和槲皮素(D + Q)的组合已被观察到可减少神经炎症、增强神经发生标志物并减轻焦虑。鉴于创伤性SCI中衰老细胞的积累,D + Q可能发挥积极的治疗作用。然而,到目前为止,D + Q治疗对促进SCI后神经功能修复的影响的研究很少。由于SCI诱导的衰老细胞位于神经实质深处,全身性、间歇性施用分子化合物可能不易穿过BSCB,因此局部施用抗衰老药物似乎是一种更有希望的方法。
在本研究中,作者首先描述了创伤引起的SCMEC衰老的表型,并深入探索了SCI后衰老SCMEC中表观遗传因素的变化。作者的研究结果表明,SCI后SCMEC中表观遗传因子UTX显著上调,并且能够靶向钙调蛋白1(CNN1)形成表观遗传调控轴。UTX/CNN1轴的缺失导致创伤引起的SCMEC衰老减少,血管功能恢复以平衡神经炎症,神经功能修复改善。此外,作者观察到局部使用抗衰老药物(D+Q)治疗可以有效减少衰老SCMEC的积累,减弱SASP分泌,并为SCI修复创造促再生微环境。
参考消息:
https://www.nature.com/articles/s41413-024-00323-x


