CLIN CANCER RES | YATAGARASU 研究:阿帕鲁胺联合戈舍瑞林治疗雄激素受体阳性涎腺癌的 2 期非随机临床试验
时间:2024-07-12 20:00:12 热度:37.1℃ 作者:网络
涎腺癌(SGC)是一种罕见且异质性的恶性肿瘤,约占头颈癌的 6%,其中,涎腺导管癌(SDC)是最具侵袭性的亚型之一,SDC 常常表达雄激素受体(AR)和人表皮生长因子受体 2(HER2),虽然 SDC 患者通常接受根治性手术和放疗,但约有一半的患者在初始治疗后 5 年内复发,近年来,针对 HER2 或 AR 的新治疗方法正在 SDC 中开发,尽管曲妥珠单抗联合多西他赛或德曲妥珠单抗在 HER2 阳性 SDC 中显示出显著的疗效,但它们仅适用于 SDC 的特定亚型,并且毒性风险相对较高,相比之下,AR 通路抑制(ARPI)可能适用于大多数 SDC,并且一些研究表明,ARPI 在 AR 阳性 SDC 中具有良好的疗效和风险效益,尤其是在联合雄激素剥夺疗法(ADT)的情况下,该研究旨在评估阿帕鲁胺联合戈舍瑞林作为 AR 阳性不可切除或复发/转移性涎腺癌(URM-SGC)的 ADT 治疗方案的有效性和安全性。

方法
这是一项在日本 7 个地点进行的开放标签、单臂、多中心 II 期研究,纳入符合条件的患者为 18 岁或以上,经组织学证实为 AR 表达的 URM-SGC,患者接受阿帕鲁胺,以 240 mg 的剂量口服,每日一次,持续给药,所有患者均接受每周期第一天皮下注射戈舍瑞林 3.6 mg 的固定剂量,方案治疗持续至疾病进展 (PD)、不可接受的毒性或撤回同意,对于出现治疗突发不良事件 (TEAE) 的患者,允许剂量中断和/或减少。主要终点是由独立中心放射学审查 (ICRR) 根据 RECIST v1.1 评估的 24 周内观察到的 24 例可评估反应患者中的总体缓解率 (ORR),次要终点包括疾病控制率 (DCR)、临床受益率 (CBR)、至反应时间 (TTR)、缓解持续时间 (DOR)、无进展生存期 (PFS)、总生存期 (OS) 和安全性。
研究结果
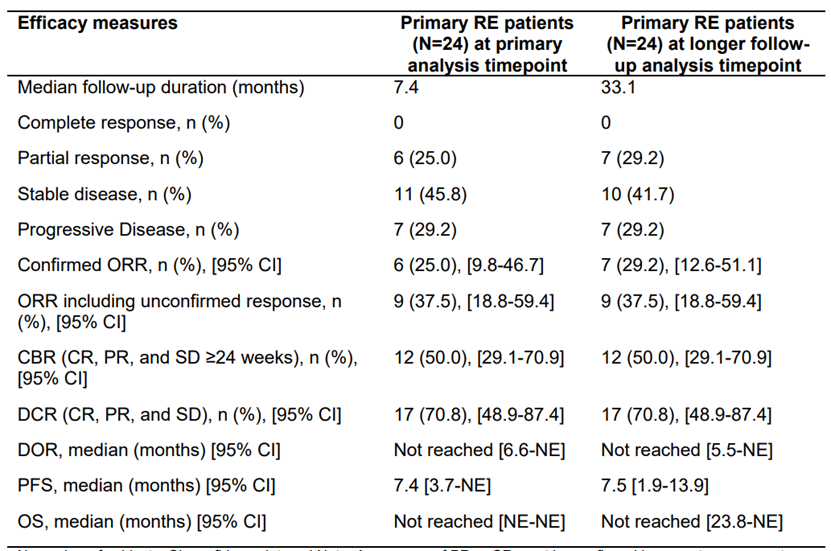
主要终点:主要可评估反应患者的 ORR 为 25.0% (6/24 名患者;95% CI: 9.8%,46.7%;P =0.11 (单侧)),未达到预先设定的疗效标准,次要终点CBR 为 50.0% (12/24;95% CI: 29.1%,70.9%),DCR 为 70.8% (17/24;95% CI: 48.9%,87.4%),中位 PFS 为 7.4 个月 (95% CI: 3.7 个月,不可估计 [NE]),中位 OS 不可估计 (NR),中位 DOR 不可估计 (95% CI: 6.6 个月,NE)。
安全性
31 名治疗患者中的 28 名 (90.3%) 经历了至少一次 TEAE,最常见的 TEAE 是皮疹;斑丘疹样皮疹 (32.3% [10/31]),皮疹 (25.8% [8/31]),口腔炎 (6.5% [2/31]) 和荨麻疹 (3.2% [1/31]),35.5% (11/31) 的患者报告了 3 级或更高的 TEAE,包括皮疹、贫血、白细胞减少和癌症疼痛,无治疗相关死亡事件报告。

结论
尽管该研究未达到预先设定的疗效标准,但阿帕鲁胺联合戈舍瑞林在 AR 阳性涎腺癌患者中显示出临床意义的疗效,并且安全性与其在前列腺癌中的先前经验一致,阿帕鲁胺联合戈舍瑞林可能成为 AR 阳性 URM-SGC 患者的一种治疗选择,尤其是对于那些 AR 表达高且无既往全身治疗史的患者。
原始出处
Honma Y, et al. 2024. Apalutamide and Goserelin for Androgen Receptor-Positive Salivary Gland Carcinoma: A Phase 2 Nonrandomized Clinical Trial, YATAGARASU. Clinical Cancer Research.


