Eur J Radiol:胶质母细胞瘤不同亚区的放射组学分割及分析
时间:2023-12-09 14:37:03 热度:37.1℃ 作者:网络
胶质母细胞瘤是最致命的原发性脑部恶性肿瘤之一,发病率为每10万人口5.26例。及时和适当的诊断可以决定未来的治疗过程,从而改善结果以及病人的生活质量。其中,MRI在其诊断和管理中起着重要作用。动态增强(DCE)灌注-MRI在胶质瘤分级中增加了价值。在过去的十年或更长时间里,研究人员专注于改进DCE灌注-MRI的技术,如改进动脉输入功能(AIF)模型、探讨在DCE灌注-MRI定量中使用实际血细胞比值而非默认值的作用以及肿瘤DCE灌注-MRI定量组织与正常外观的实质组织的正常化。与作为基础事实的组织病理学相比,每一项发展都改善了疾病分类和分级。
不同等级的胶质瘤的行为及其对成像指标的影响是复杂的,往往不能通过增强后的T1加权图像上的增强或不增强来统一表达。有报道称,低等级胶质瘤的增强和高等级的不增强是矛盾的。此外,还有一些特征,如坏死和水肿也起着同样重要的作用。肿瘤亚区的边界(水肿、坏死、增强和非增强亚区)往往是重叠的,放射科医生在绘制分割图时是无法区分的。然而,这些亚区在给定的胶质瘤环境中如何表现的时间轨迹可以提示这些可能的进展或对治疗的反应[。最近,研究人员实施了基于机器学习的半自动算法,利用DCE灌注-MRI成像方法(Ktrans、rCBV、rCBF、ve),提取肿瘤特征-区间边界和相关的子区间体积。这些特征与胶质瘤等级高度相关,并显示出低分类误差的临床前景。
DCE灌注-MRI在扫描采集、造影剂注射和复杂的算法设计方面计算量很大。每一项技术改进都是确定子室边界/体积/数量的重要因素,因此在全球范围内实施连续修改具有挑战性。因此,子室边界的微小差异会对分级系统产生重大影响。
放射组学分析和特征提取本质上是一种计算方法,可用于描述细微的潜在的解剖学、病理学和定量变化。研究证明了放射学分析在预测胶质母细胞瘤假性进展方面的能力以及结合DWI和灌注放射学分析来预测低级别胶质瘤患者的生存率。基于DCE灌注-MRI参数图的瘤内和瘤周放射组学特征已被证明可以高度准确地预测乳腺癌肿瘤的HER-2和Ki-67状态。

近日,发表在Eur J Radiol杂志的一项研究探索了从DCE灌注-MRI指标得出的胶质瘤亚区在三维强化后T1和三维FLAIR图像上进行放射组学分析的可行性,并将放射组学特征特征组合成一个预测模型在没有DCE灌注-MRI的情况下进行亚区划分及分析。
本项研究共纳入了89名组织病理学证实为IDH野生型的GB患者,所有患者均接受了DCE灌注MRI的MR成像。计算灌注指数和动力学指数,并进一步用于分割肿瘤亚区。用PyRadiomics工具从FLAIR和T1GD图像中提取放射组学特征。使用两种方法对这些特征进行统计分析,并分别构建了机器学习(ML)模型,i)在不同的肿瘤亚区,ii)ED作为一个类别,其余亚区合并为另一个类别。同时还构建了基于ML的预测性特征图。
在FLAIR和T1GD图像中,发现有7个特征对区分肿瘤亚区具有统计学意义,P值<0.05,AUC值在0.72至0.93之间。在第二种方法中,ML模型能够将FLAIR和T1GD图像中的ED从其他肿瘤亚区中分类出来,AUC分别为0.95和0.89。
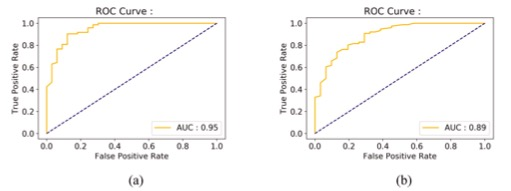
图 使用ED区和ET、NET和NEC区的重要放射组学特征训练的基于RF的ML模型的ROC图以区分ED和其他肿瘤区域,(a)FLAIR图像的ROC图显示AUC为0.95,(b)T1GD图像的ROC图显示AUC为0.89
本项研究表明,基于放射组学的特定特征值有助于描述不同肿瘤亚区的影像学特征,这对未来使用常规MRI对水肿与肿瘤进行分割具有重要的临床价值。
原文出处:
Suhail Parvaze,Rupsa Bhattacharjee,Anup Singh,et al.Radiomics-based evaluation and possible characterization of dynamic contrast enhanced (DCE) perfusion derived different sub-regions of Glioblastoma.DOI:10.1016/j.ejrad.2022.110655


