ALK 新思享|高天教授:恩沙替尼成功治疗晚期炎性肌纤维母细胞瘤,患者持续长期缓解!
时间:2023-11-06 00:55:47 热度:37.1℃ 作者:网络
编者按:我国原研ALK-TKI恩沙替尼上市后为我国ALK融合阳性肿瘤患者带来了良好的疗效,也带来了新的实践经验。实践是最好的老师,为了更好的使用恩沙替尼为患者进行治疗,【ALK新思享】将分享来自一线对原研ALK-TKI恩沙替尼在临床实践中的临床感悟和思考。
医悦汇:您有一例晚期炎性肌纤维母细胞瘤治疗后pCR的病例,请分享这例患者的情况及诊疗过程。
高天教授:很高兴和大家分享一例我们科室通过使用ALK抑制剂恩沙替尼治疗后达到病理完全缓解的炎性肌纤维母细胞肉瘤病例。
我们成功治疗的是一位38岁的年轻女性患者,具有纤维肉瘤癌症家族史,在2022年10月时,因腹痛、腹胀在当地医院就诊,胸腹盆部CT提示,左肺下叶背段占位,大小约4.6cm×3.5cm,盆腔部分空肠套叠,近端空肠梗阻。于是在当地行医院全麻下接受了腹腔镜探查术、部分肠管切除吻合术,术中肿物探查约为5cm×4cm×4cm,术后病理提示,肿瘤呈现圆细胞和卵圆细胞,考虑BCOR融合肉瘤,获取的5个肠系膜淋巴结中有4个为转移的淋巴结。2022年12月时,患者在山西省肿瘤医院进行PET-CT检查,结果提示:左肺下叶代谢增高肿物,肿瘤大小为8.9cm×7.2cm,考虑出现了恶性肿瘤转移。为了进一步治疗,患者来到了我院门诊就诊。我院增强CT提示,患者左肺下叶背段支气管狭窄,远端见软组织肿块,大小约95mm×73mm,结合病史,考虑出现转移的可能性较大。
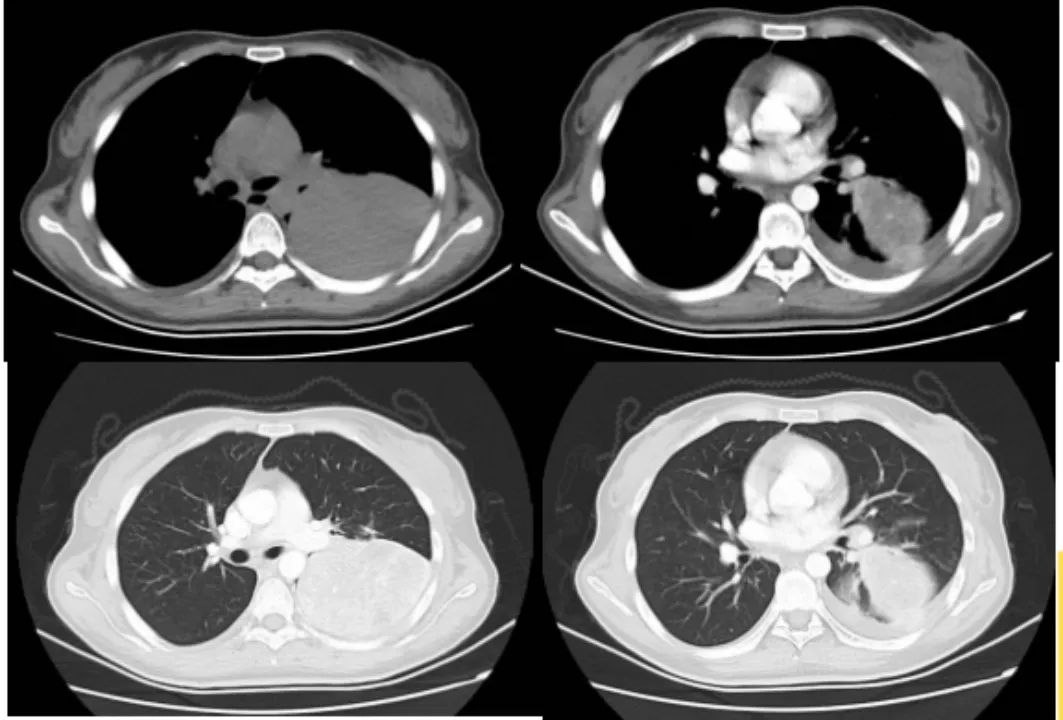
增强CT显示:左肺下叶背段支气管狭窄,远端见软组织肿块,大小约95x73mm
为了更好的进行治疗,我们进行了详细的检查。结合病理和免疫组化结果,考虑为上皮样炎性肌纤维母肉瘤(EIMS),且恶性程度高,ki67高达 60%。基因检测提示:患者存在EML4-ALK 融合;PD-L1表达检测为TPS 40%,CPS 41。最终诊断为:小肠上皮样炎性肌纤维母细胞瘤术后 ALK-EML4;左肺下叶转移瘤;T2N0M1 G3 IV期。
众所周知,炎性肌纤维母细胞肉瘤是软组织肉瘤中非常罕见的亚型。目前,查阅指南发现,对于晚期软组织肉瘤,尚缺乏高效的特异性靶向药物治疗。鉴于相比靶向治疗,化疗的副作用更大,因此,为了保证患者的生活质量,同时,结合患者的基因检测结果,我们初步确认患者可以不接受长疗程的化疗,并且有条件将ALK抑制剂作为主要治疗手段。
而恩沙替尼是一种新型强效、高选择性的新一代 ALK 抑制剂。此前被NMPA批准,用于接受过克唑替尼治疗后进展的或对克唑替尼不耐受的ALK阳性的局部晚期或转移性NSCLC的治疗。
鉴于该患者病情属晚期高危,一代二代测序ALK融合明确,建议口服恩沙替尼,以期尽可能的延长患者的生命,并争取手术机会。
在第一个治疗周期,给予患者口服恩沙替尼225mg Qd,用药3天后自觉好转,在经过一个月靶向治疗后,患者呼吸压迫症状得到明显的缓解,胸部CT提示肿瘤明显缩小,从原来的9cm退缩到2-3cm。总体感觉,尽管患者确诊时已经出现转移,但恩沙替尼的治疗效果出乎我们的预期。
特别是在经过5个月的治疗后,影像结果表明,患者左肺仅余两个小肿瘤,且前纵隔肿物较前明显减小60%,术前评效达到PR。值得一提的是,从开始治疗到5个月后,整体治疗过程非常顺利。除了偶尔的干咳,几乎没有出现其他明显副作用,患者的症状也明显好转。
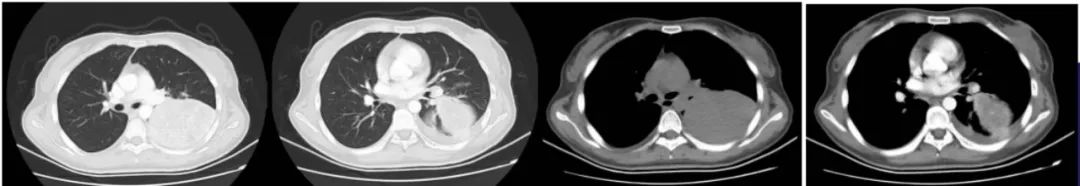
治疗前
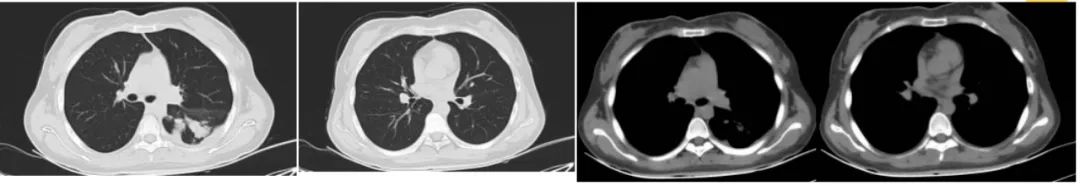
治疗1个月后
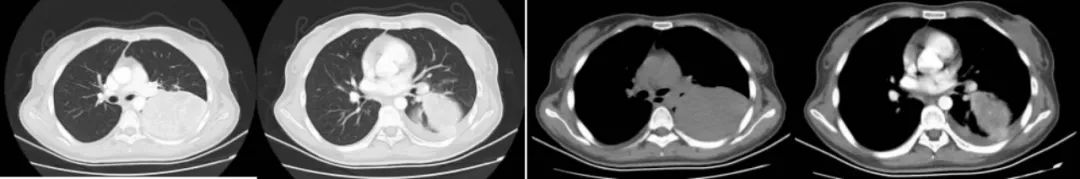
治疗前影像评效:PR
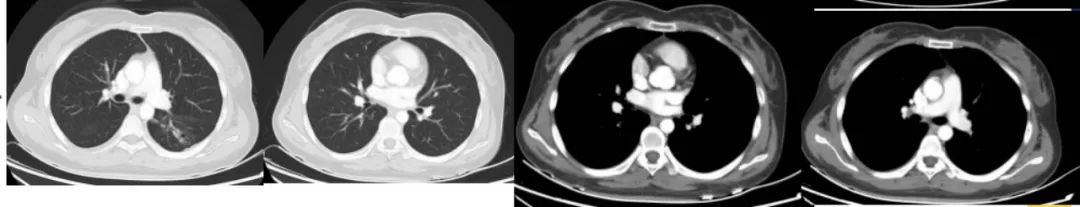
治疗3个月后影像评效:PR

治疗5个月后影像评效:PR
在此基础上,我们再次进行了多学科讨论,考虑到疗效如此显著,我们决定尝试帮助患者达到完全缓解状态,争取无瘤状态。
由于患者年纪较轻,体质良好,接受胸腔镜手术基本没有什么禁忌。于是在2023年6月7日,即患者口服恩沙替尼5个月后,进行了手术治疗(胸腔镜下左肺下叶楔形切除+胸腔闭式引流术)。术中发现病灶与胸膜粘连侵犯,分离并切除了胸膜病灶。
左肺下叶切除的两个肿物大小分别2cm和2.5cm,术后肺组织标本病理报告显示,未发现恶性肿瘤细胞。这意味着所有的肿瘤细胞都已被药物治疗清除,达到了病理完全缓解(pCR)。
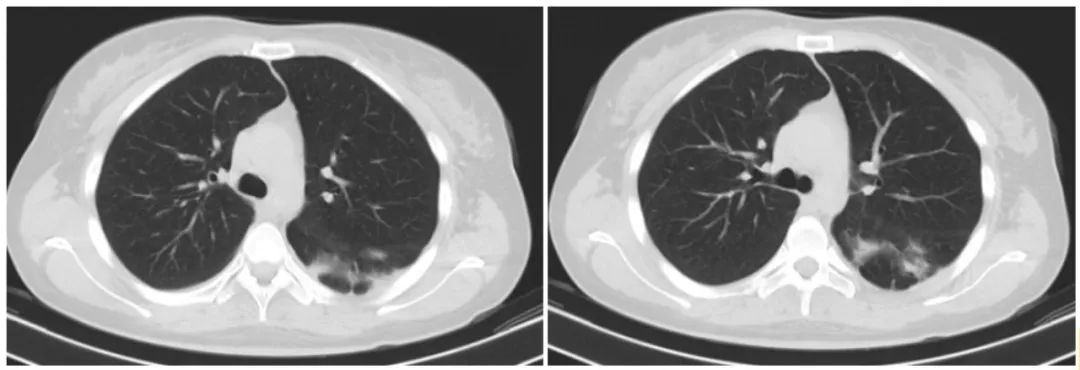
术前多学科评估:左肺下叶肿块较前明显缩小
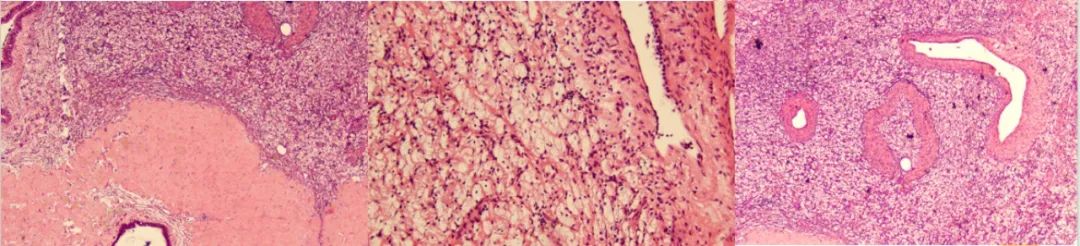
回顾患者的治疗经历,首先,晚期软组织肉瘤在经过ALK抑制剂的药物转化治疗后,为患者创造了根治性手术机会。其次,患者术前靶向治疗效果显著,达到了pCR,这在肉瘤治疗中非常罕见。另外,经过多学科讨论我们发现,患者并非简单的炎性肌纤维母细胞肉瘤,而是具有高度侵袭性的上皮样炎性肌纤维母细胞肉瘤(EIMS)。
EIMS是恶性炎性肌纤维母细胞瘤(IMT)的上皮样亚型,其特点是具有高度侵袭性生物学行为,并且容易转移和复发,这一点与患者的症状也非常贴合。腹腔是EIMS的好发部位(约84%),发病中位年龄34岁,且常见有特征性的RANBP2-ALK和和RRBP1-ALK基因融合。文献报道,与传统的IMT相比,EIMS较早出现复发及转移,预后不佳。
患者的情况是EIMS转移到肺上,并有ALK-EML4基因融合,侵袭性比较强。据文献报道,相比普通的IMT,EIMS病情更加的凶险,愈后也相对更差。通过此次这例EIMS患者的成功治疗,我们发现部分肉瘤患者尤其是存在ALK-EML4基因融合的EIMT患者,有望通过ALK抑制剂得到获益。不仅可以延长生存期,还可能通过ALK抑制剂治疗,将肿瘤缩小后再进行手术治疗,达到无瘤状态的长期生存。
医悦汇:EIMS的诊疗现状是怎样的?哪些亚型的肉瘤患者能ALK-TKI中获益?
高天教授:EIMS被称为上皮样炎性肌纤维母细胞肉瘤,是炎性肌纤维母细胞瘤的一种。在ALK抑制剂出现之前,我们主要依赖的治疗手段是化疗,还有常规的抗血管生成小分子靶向药物。
然而,传统的化疗往往给患者带来巨大的痛苦,并且疗效有限,难以耐受化疗相关的白细胞减少、肝功能异常及血小板减少等问题。此外,抗血管生成靶向治疗的疗效也相对有限,肿瘤缩小率仅有10%左右。
而这例患者在使用ALK抑制剂后,症状明显缓解(PR),让我们看到,有针对性的靶向治疗比没有针对性的化疗或者小分子TKI治疗效果更好。当然,只有在经过基因检测,并确定患者存在ALK融合时,才会选择使用ALK抑制剂。ALK突变除了融合还有其他基因改变形式,如基因扩增和其他突变类型。
从既往的文献报告中,ALK抑制剂主要对存在基因融合和重排的病例有效。我们这位患者恰好有融合和重排,所以,使用ALK抑制剂恩沙替尼治疗效果非常好。
医悦汇:对比其他 ALK-TKI,您选择恩沙替尼作为临床治疗药物是出于怎样的考虑?本例肺转移患者目前为全身无瘤状态,是否继续服用ALK抑制剂,服用多久?
高天教授:当面对ALK治疗方案的选择时,团队内部进行了深入的讨论。最初在选择恩沙替尼时,确实有些犹豫。
回顾既往文献,针对肉瘤的临床试验主要是克唑替尼。试验发现,克唑替尼在IMT中ALK融合基因亚型里有50%患者达到了PR,表明药物起到了效果;而另外50%的患者则保持疾病稳定,表明整体控制不错。此前,我们尝试过使用克唑替尼进行治疗,发现特别是儿童患者恶心呕吐的不良反应较重,甚至达到无法服用药物的程度。因此,即使知道克唑替尼对部分患者有效,但副作用的影响让很多患者无法接受,所以就没有考虑克唑替尼治疗。
我们非常希望帮助患者制定一套“既能尽量克服耐药性,同时不良反应小,且经济上可以被患者接受”的治疗方案。二代ALK-TKI恩沙替尼在ALK阳性NSCLC的治疗中表现出色,安全性好,且成为这部分人群的首选治疗方案。实际上,克唑替尼和恩沙替尼在肉瘤中都没有获批的适应症,这意味着两个药物治疗肉瘤的循证证据级别是相同的,由于恩沙替尼相对克唑替尼的价格更低,且安全性更好,基于上述考虑,最终推荐恩沙替尼给患者作为治疗方案。
目前,患者已经达到了pCR,且体内无瘤。在决策关于特异性靶向药的使用时长时,我们参照了胸内科和胸外科的意见。实际上,在处理晚期肺癌患者时,也面临类似的选择——患者达到完全缓解后是否需要长期服药。
尽管医学指南并没有明确指出具体的服用时长,但从医生的经验来看,主要有两个考虑因素:首先,患者的经济状况。恩沙替尼的费用相对较低,还有赠药政策,在很大程度上减轻了患者的经济负担。其次,关注药物的不良反应,患者反馈在服用恩沙替尼时几乎没有感受到任何不良反应。因此,结合患者的经济状况和对药物不良反应的反馈,建议至少继续服药一年。基于目前的状况是服药一年,一年后会再次复查,并根据当时状况作出进一步的决策。
医悦汇:这例应用恩沙替尼治疗EML4-ALK融合炎性肌纤维母细胞瘤患者的临床价值和指导意义有哪些,带来哪些新的思考?
高天教授:应用恩沙替尼成功治疗EML4-ALK融合炎性肌纤维母细胞瘤的经历,让我对肉瘤的靶向治疗更有信心了。以往,肉瘤的治疗常采用抗血管生成小分子靶向药物,然而,广谱靶向药并不是真正的点对点的靶向治疗。在临床实践中我们发现,抗血管生成小分子靶向药物治疗的客观反应率并不高,且对患者的损伤较大,为软组织肉瘤的整体治疗带来了困扰。所以,我们也迫切希望有更多的不良反应小,价格低廉,且有针对性的治疗方案提供给患者。
这例患者未接受常规化疗和靶向治疗,直接进行了点对点的靶向治疗,并取得了令人鼓舞的效果。这为我们提供了新的思路——只要找到正确的治疗方案,就能为患者带来更大获益。特别是年轻肉瘤患者的治疗,更需要得到大家的关注,未来要继续朝着不良反应小、疗效好的治疗方向研究。
值得一提的是,EML4-ALK阳性或ALK基因融合的患者首选ALK抑制剂治疗。除了ALK以外,软组织肿瘤还有一些特殊的基因,如NTRK1、NTRK2、NTRK3、基因突变及扩增,还有Mtor抑制剂,都可以进行尝试和探索,以期为更多肉瘤患者提供更好的更有针对性的治疗。


