FDA 上半年批准的新药汇总
时间:2023-07-14 17:11:51 热度:37.1℃ 作者:网络
今天汇总一下FDA上半年批准的新药,共26款,Q1和Q2各13款,要显著多于去年上半年的16款。其中辉瑞表现强劲,获得三款新药批准。
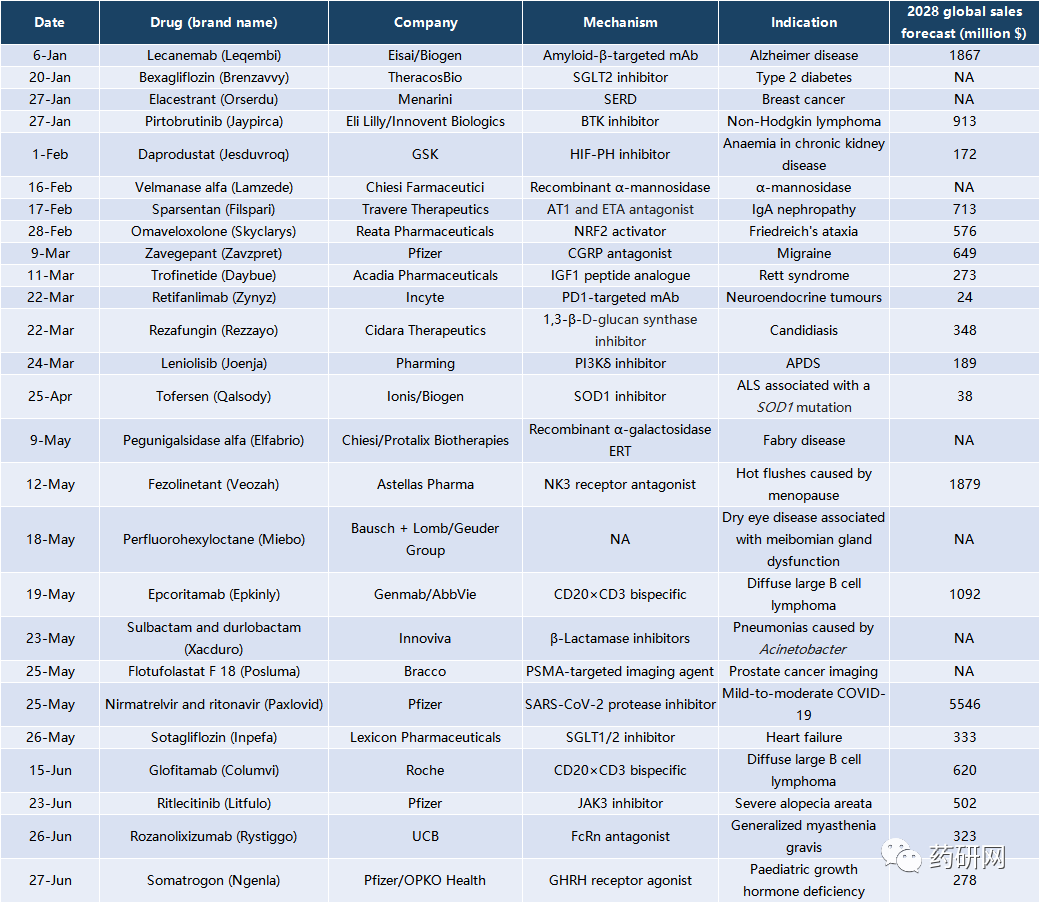
数据来源:Nature Reviews Drug Discovery; EvaluatePharma
预计到2028年将有4款重磅炸弹:Paxlovid、Veozah、Lequmbi和Epkinly。
Paxlovid此前获得紧急使用,在今年五月正式获得了全面批准,但随着疫情的减缓,人们对新冠药需求的降低,其销售额预计会从2022年的189亿美元峰值降至2028年的55亿美元。
Veozah是安斯泰来的NK3受体拮抗剂,原研公司为Ogenda,该公司于2017年被安斯泰来收购。原定PDUFA目标日期是2月22日,后FDA延长至5月22日。Veozah是首款治疗更年期潮热的非激素疗法,预计2028年销额会达18.8亿美元。
卫材/Biogen的Leqembi在1月获加速批准上市,7月6日进一步获得完全批准,成为20年来首款获完全批准的阿尔兹海默症新药,定价2.65万美元/年。预计2028年全球销额会达到18.7亿美元,但这是在加速批准的基础上,完全批准后,美国医疗保险与医疗补助服务中心(CMS)会扩大覆盖范围,市场渗透率会进一步提高。
此外,上半年获批的两款双抗均是CD3/CD20双抗,分别是艾伯维/Genmab的Epkinly和罗氏的Columvi,适应症均是弥漫性大B细胞淋巴瘤(DLBCL)。
DLBCL是最常见的非霍奇金淋巴瘤类型。据估计,2022年美国该病患者达3.04万例,而全球每年新增病例多达15万例。
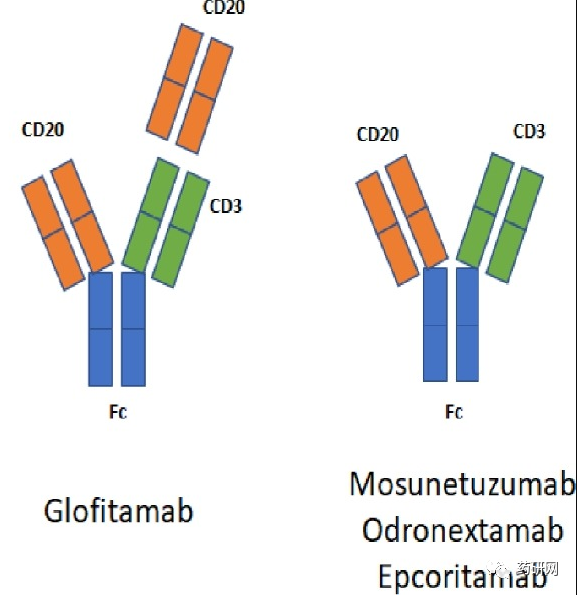
https://doi.org/10.1016/j.lrr.2021.100282
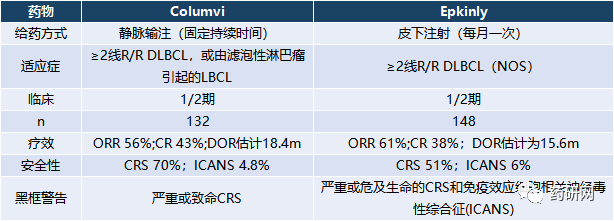
Epkinly的预期销额要高于Columvi,主要是基于Epkinly的疗效、给药方式和安全性。
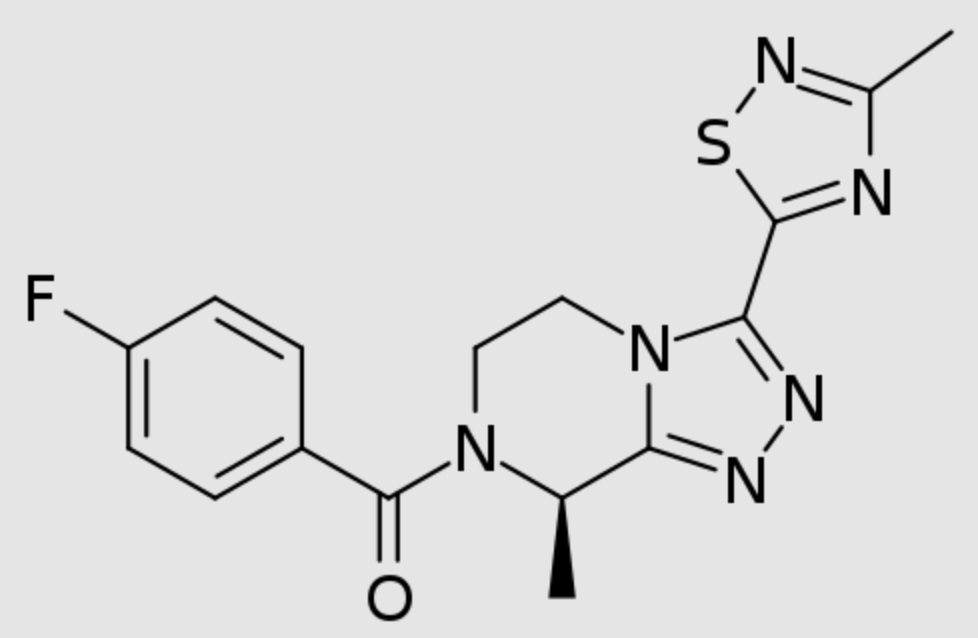
礼来的BTK抑制剂Jaypirca预计2028年销额达到9.1亿美元,这是FDA批准的首款也是唯一一款非共价BTK抑制剂,在此之前获批的五款均为共价抑制剂,获批用于治疗经过至少两线系统治疗(包括其他BTK抑制剂)的复发性或难治性套细胞淋巴瘤(MCL)成年患者。
虽已上市多款抑制剂,竞争激烈,但共价抑制剂会出现安全性或耐药的问题,而Jaypirca可用于其他BTK抑制剂治疗后进展的患者,同时安全性有所提高。
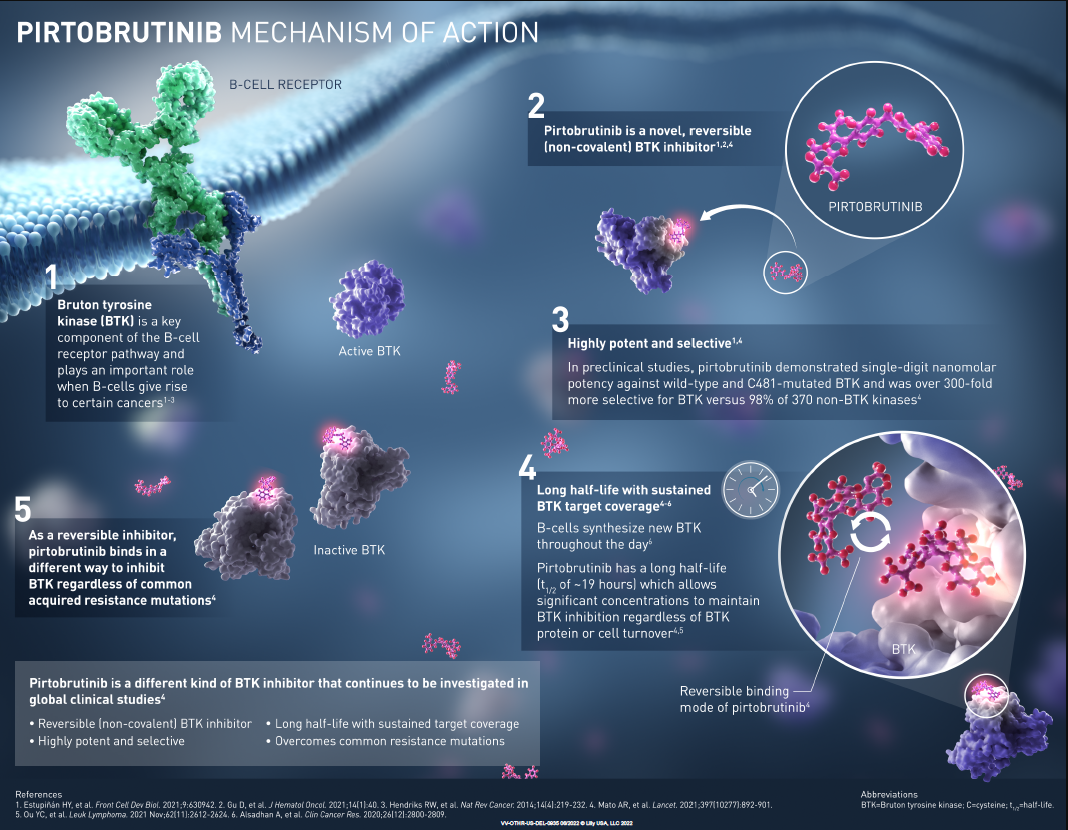
Jaypirca作用机制
还有一些“第一”:
-
Reata公司的NRF2激动剂Skyclarys(omaveloxolone)是首个治疗退行性神经肌肉疾病弗里德赖希共济失调症(FA)的产品,此前几十年都未曾有药物成功,而这款药的获批也是一波三折,从2020年被推迟后直到23年才成功获批;
-
Acadia的IGF-1肽类似物Daubue是首个治疗Rett综合征的药物;
-
Menarini治疗乳腺癌的药物Orserdu是获批的首个口服SERD,在此之前,阿斯利康的氟维司群(fulvestrant)是唯一获批上市的 SERD 靶向药,只能肌肉注射。
-
Chiesi的Lamzede是首个在美批准治疗α-甘露糖苷贮积症(AM)的非中枢神经系统表现的酶替代疗法;
-
Pharming的PI3Kδ抑制剂Joenja是首款用于APDS(一种原发性免疫缺陷病)治疗的药物,但该药受众相对较少,在美国仅发现了200名患者;
-
辉瑞的Zavzpret是首个治疗偏头痛的CGRP受体拮抗剂鼻腔喷雾,15分钟即可发挥效果,此前8款CGRP/CGRPR类偏头痛药物均为口服。
-
Cidara的棘白菌素类药物Rezzayo十多年来首个批准用于念珠菌血症和侵袭性念珠菌病患者的新治疗方案。
从这些第一中我们可以了解,在上半年获批的药物中,有多款药打破了其治疗领域“无药可用,无药可医”的困局,让众多的罕见病患者有了希望。目前有很多罕见病,人们对其知之甚少,相关研究也不多,但随着近几年药企对罕见病研发投入的加大,相信越来越多的罕见病人终有一天会被看见,会得以被治疗。而有药可医的背后,也少不了研发团队多年的坚持。
还值得一提的是,26款药物中预计销额最低的药物是Incyte的PD1单抗 Zynyz,这是FDA批准的第五款PD1单抗,治疗默克尔细胞癌(MCC),而Zynyz并不是第一款获批MCC的PD1/PDL1抑制剂,较低的预估销额主要是因为激烈的竞争。
参考:
1.https://www.nature.com/articles/d41573-023-00065-1.
2.https://www.nature.com/articles/d41573-023-00117-6.


